写出下列反应的化学方程式,并在括号内注明基本反应类型:
(1)铁丝在氧气中燃烧 (__________)反应
(2)酒精(C2H5OH)在空气中燃烧
(3)铁在高温下和水蒸气发生化学反应生成四氧化三铁和另外一种可燃性气体单质 .
下图为元素周期表的一部分,请按要求填空:
(1)氢元素与氦元素的本质区别是。
(2)表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的相同。
(3)表中9号和17号元素化学性质相似的原因是。钠元素和氟元素组成的化合物的化学式为。
化学基础知识是学好化学的关键,请按下列要求填空.
(1)请用化学符号填空:
①两个氢分子 ;②铵根离子 .
(2)图1是某微粒的结构示意图.其中X= .该微粒在化学反应中易 (填“得”或“失”)电子;写出一条从图2中获得的信息 .
(3)如图3所示是汽车尾气治理过程中某反应的微观示意图.请按要求回答问题.
①图3中体现了在化学变化前后一定不变的是 (填序号).
| A.元素种类; | B.原子种类; | C.分子数目; | D.原子数目. |
②图3中发生反应的化学方程式为
水、食品和空气都与人类息息相关,它们的安全问题影响到人类的生存、健康。
(1)2012年“世界水日”的主题是“水与粮食安全”,下列做法正确的是( )
| A.任意排放未经处理的生活污水 | B.加大农药的使用量,以减少昆虫的危害 |
| C.禁止使用含磷洗衣粉 | D.用硫酸铜给饮用水消毒 |
(2)长期饮用硬水对人体健康不利,生活中可用来区别硬水和软水;高铁酸钠(Na2FeO4)是一种新型高效的净水剂,高铁酸钠中铁元素的化合价为。
(3)用工业明胶制成的医用“毒胶囊”中混有的重金属铬对人体有害。这里的铬是指
(填“元素”或“单质”)。
(4)①空气中的氮气和氧气在放电的条件下能生成一氧化氮。请写出该反应的化学方程式。
②目前,有一种治理废气中一氧化氮的方法,其反应的化学方程式为:
4NH3+6NO  5N2+6X。则X的化学式为。
5N2+6X。则X的化学式为。
选择氧气、二氧化碳、金刚石、氮气的化学式填空:
(1)能用于灭火的气体是 ;
(2)可用作食品保护气气体是 ;
(3)自然界中存在最硬的物质 ;
(4)不能燃烧,但能支持燃烧的气体是 ;
在实验室中利用下图装置,可以进行的实验是()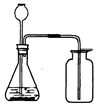
| A.用过氧化氢溶液与MnO2制取氧气 |
| B.用KMnO4固体制取氧气 |
| C.用KClO3与MnO2的混合物制取氧气 |
| D.用石灰石与稀盐酸制取二氧化碳气体 |