氮及其化合物在生活、生产和科技等方面有重要的应用。砷位于周期表中的第四周期,与氮元素属同一主族元素,其广泛分布与自然界。试回答下列问题:
(1)砷的气态氢化物的电子式为 。
(2)氨和联氨(N2H4)是氮的两种常见化合物,制备联氨可用丙酮做催化剂,将次氯酸钠与氨气反应,该反应中还原剂与氧化剂的物质的量之比为2:1,写出该反应的化学方程式: 。
(3)砷的常见酸性氧化物有As2O3和As2O5,请根据图相关信息写出分解为的热化学方程式: 。
(4)直接供氨式碱性燃料电池的电池反应式为4NH2+3O2=2N2+6H2O,电解 质溶液一般使用氢氧化钾溶液,则负极电极反应式为 。
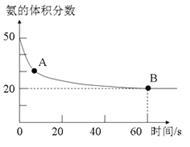
(5)氨气和二氧化碳在120℃,催化剂作用下反应生成尿素:CO2(g)+2NH3(g) 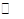 (NH2)2CO(s)+H2O(g),在密闭反应容器中,混合气体中氨气的含量变化关系如图所示,则氨气的平衡转化率是 。
(NH2)2CO(s)+H2O(g),在密闭反应容器中,混合气体中氨气的含量变化关系如图所示,则氨气的平衡转化率是 。
(6)将一定量的NH2COONH4(s)置于恒温密闭容器中,NH2COONH4(s) 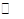 2NH3(g)+CO2(g),其分解达到平衡状态时,该反应的化学平衡常数的表达式为 。
2NH3(g)+CO2(g),其分解达到平衡状态时,该反应的化学平衡常数的表达式为 。
(7)在容积恒定的密闭容器中进行反应2NO(g)+O2(g) 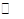 2NO2(g) △H>0,该反应的反应速率(v)随时间(t)变化的关系如图所示,若t2、t4时刻只改变一个条件,下列说法正确的是 (填序号)
2NO2(g) △H>0,该反应的反应速率(v)随时间(t)变化的关系如图所示,若t2、t4时刻只改变一个条件,下列说法正确的是 (填序号)
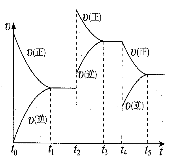
a.在t1-t2时,可依据容器内气体的压强保持不变判断反应已达到平衡状态
b.在t2时,采取的措施可以是升高温度
c.在t3-t4时,可依据容器内气体的密度保持不变判断反应已达到平衡状态
d.在t5时,容器内NO2的体积分数是整个过程中的最大值
三氟化氮(NF3)是一种无色无味的气体,可由氟与氨反应制得。
(1)该反应的方程式为NH3+F2→NF3+NH4F,配平方程式并标明电子转移的方向和数目。
(2)27.0 mL NF3和水充分反应,生成 18.0 mL NO(同温、同压下),写出反应的化学方程式:___________________________________。
(3)NF3是一种无色无味的气体,但一旦NF3在空气中泄漏,还是易于发现的。该气体泄漏时的现象是。
20 g烧碱配制成500 mL溶液,其物质的量浓度为________mol·L-1;从中取出1 mL,其物质的量浓度为________mol·L-1,含溶质______g。若将这1 mL溶液用水稀释到100 mL,所得溶液中溶质的物质的量浓度为__________mol·L-1,其中含Na+______g。
(1)金属镁有许多重要的用途,法国化学家维多克·格利雅因发明了在有机合成方面用途广泛的格利雅试剂而荣获诺贝尔化学奖,格利雅试剂的结构简式可表示为RMgX,它是金属镁和卤代烃反应的产物,简称格氏试剂,它在醚的稀溶液中以单体形式存在,并与二分子醚络合,在浓溶液中以二聚体存在,结构如下图: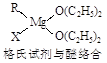
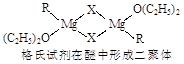
①上述2种结构中均存在配位键,把你认为是配位键的用“→”标出。
②由原子间的成键特点,可以预测中心原子Mg的杂化类型可能为______;Mg 原子的核外电子排布式可表示为______________________。
③下列比较中正确的是____________
A.金属键的强弱:Mg>Al B.基态原子第一电离能:Mg>Al
C.金属性:Mg>AlD.晶格能:NaCl>MgCl2
(2)将TiCl4在氩气保护下与镁共热得到钛:
TiCl4+2Mg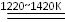 Ti+2MgCl2
Ti+2MgCl2
①Ti元素在元素周期表中的位置是,钛原子的外围电子排布式为。
②TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟。则TiCl4属于(填“原子”、“分子”或“离子”)晶体。
③二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体转化为二氧化碳和水,达到无害化。有关甲醛、苯、二氧化碳及水,下列说法正确的是。
A.苯与B3N3H6互为等电子体
B.甲醛、苯分子中碳原子均采用sp2杂化
C.苯、二氧化碳是非极性分子,水和甲醛是极性分子
D.水的沸点比甲醛高得多,是因为水分子间能形成氢键
(3)2001年报导的硼和镁形成的化合物刷新了金属化合物超导温度的最高纪录。下图中示意的该化合物的晶体结构单元:镁原子间形成正六棱柱,在棱柱的上下底面还各有一个镁原子,六个硼原子位于棱柱内,则该化合物的化学式可表示为。(填字母选项)
A.MgB B.MgB2 C.Mg2B D.Mg3B2
地球的海水总量约有1.4×1018t,是人类最大的资源库。
(1)如右图利用海水得到淡水的方法为。
(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如右下图。a是电源的 极;Ⅰ口排出的是 (填“淡水” 或“浓水”)。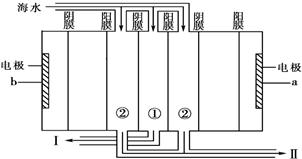
(3)海水淡化后的浓水中含大量盐分(主要含有Mg2+、 Ca2+、Fe3+和SO42-),排入水中会改变水质,排到土壤中会导致土壤盐碱化,故不能直接排放,可以与氯碱工业联产。电解前需要把浓水精制,所需试剂主要包括:HCl、NaOH、 BaCl2、Na2CO3等),其中HCl的作用主要是
(4)铀是核反应最重要的燃料,其提炼技术直接关系着一个国家核工业或核武器的发展水平,海水中铀以UCl4形式存在(以离子形式存在),每吨海水只含3.3毫克铀,海水总量极大,铀总量相当巨大。不少国家正在探索海水提铀的方法。现在,已经研制成功一种螯合型离子交换树脂,它专门吸附海水中的铀,而不吸附其他元素。其反应原理为:___________________________(树脂用HR代替),发生离子交换后的离子交换膜用酸处理还可再生并得到含铀的溶液,其反应原理为:________________________。
(5)离子交换树脂法是制备纯水(去离子水)的主要方法。某阳离子交换树酯的局部结构可写成(右图)。该阳离子交换树脂是由单体苯乙烯和交联剂对二乙烯基苯聚合后再经__ 反应得到的。自来水与该离子交换树脂交换作用后显 (填“酸性”、“碱性”或“中性”)。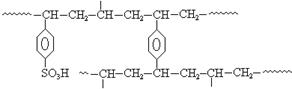
(6)中国《生活用水卫生标准》中规定,水的总硬度不能过大。如果硬度过大,饮用后对人体健康与日常生活有一定影响。暂时硬水的硬度是由(填阴离子符号)引起的,经(填操作名称)后可被去掉。永久硬水的硬度可由离子交换法去掉。
水是人类生存和发展的宝贵资源,而水质的污染问题却越来越严重。目前,世界各国已高度重视这个问题,并采取积极措施进行治理。
(1)下列项目:色度、浊度、pH、某些金属离子、氯离子、硫酸根离子、氮和磷的化合物、、生化需氧量等都是评价水质需要检测的项目,其中生化需氧量主要是检测水体中(填“哪类物质”)消耗氧气的量。
(2)工业废水中常含有不同类型的污染物,可采用不同的方法处理。以下处理措施和方法都正确的是________(填字母编号,可多选)。
| 选项 |
污染物 |
处理措施 |
方法类别 |
| A |
废酸 |
加生石灰中和 |
物理法 |
| B |
Cu2+等重金属离子 |
加硫酸盐沉降 |
化学法 |
| C |
含纯碱的废水 |
加石灰水反应 |
化学法 |
(3)下图是某市污水处理的工艺流程示意图: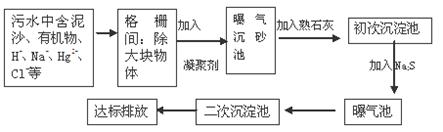
①下列物质中不可以作为混凝剂(沉降剂)使用的是(填字母编号,可多选)。
A.偏铝酸钠 B.氧化铝 C.碱式氯化铝 D.氯化铁
②混凝剂除去悬浮物质的过程是(填字母编号)。
A.只是物理过程 B. 只是化学过程 C. 是物理和化学过程
(4)在氯氧化法处理含CN一的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质。
某厂废水中含KCN,其浓度为650 mg·L-1。现用氯氧化法处理,发生如下反应:
KCN + 2KOH + Cl2 =" KOCN" + 2KCl + H2O再投入过量液氯,可将氰酸盐进一步氯化为氮气。请配平下列化学方程式:口KOCN + 口KOH + 口Cl2→ 口CO2 + 口N2 + 口KCl + 口H2O若处理上述废水20L,使KCN完全转化为无毒物质,至少需液氯g。