室温下,向下列溶液中通入相应的气体至溶液pH=7(通入气体对溶液体积的影响可忽略),溶液中部分微粒的物质的量浓度关系正确的是
| A.向0.10mol·L-1NH4HCO3溶液中通入CO2:c(NH4+)=c(HCO3-)+c(CO32-) |
| B.向0.10mol·L-1NaHSO3溶液中通入NH3:c(Na+)>c(NH4+)>c(SO32-) |
| C.0.10mol·L-1Na2SO3溶液通入SO2:c(Na+)=2[c(SO32-)+c(HSO3-)+c(H2SO3)] |
| D.0.10mol·L-1CH3COONa溶液中通入HCl:c(Na+)>c(CH3COOH)=c(Cl-) |
下列说法中不正确的是()
| A.化石燃料在任何条件下都能充分燃烧 |
| B.化石燃料在燃烧过程中能产生污染环境的CO、SO2等有害气体 |
| C.直接燃烧煤不如将煤进行深加工后,再燃烧效果好 |
| D.固体煤变为气体燃料后,燃烧效率将更低 |
已知下列热化学方程式
Zn(s)+ 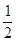 O2(g)====ZnO(s) ΔH1="-351.1" kJ·mol-1
O2(g)====ZnO(s) ΔH1="-351.1" kJ·mol-1
Hg(l)+ 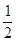 O2(g) ====HgO(s) ΔH2="-90.7" kJ·mol-1
O2(g) ====HgO(s) ΔH2="-90.7" kJ·mol-1
由此可知Zn(s)+HgO(s) ====ZnO(s)+Hg(l) ΔH3。其中ΔH3的值是()
| A.-441.8 kJ·mol-1 | B.-254.6 kJ·mol-1 |
| C.-438.9 kJ·mol-1 | D.-260.4 kJ·mol-1 |
下列热化学方程式书写正确的是()
A.2SO2+O2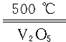 2SO3 ΔH="-196.6" kJ·mol-1 2SO3 ΔH="-196.6" kJ·mol-1 |
B.H2(g)+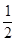 O2(g)====H2O(l) ΔH="-285.8" kJ·mol-1 O2(g)====H2O(l) ΔH="-285.8" kJ·mol-1 |
| C.2H2(g)+O2(g) ====2H2O(l) ΔH="-571.6" kJ |
| D.C(s)+O2(g) ====CO2(g) ΔH="+393.5" kJ·mol-1 |
已知在298 K、1×105 Pa条件下,2 mol 氢气燃烧生成水蒸气放出484 kJ的热量,下列热化学方程式正确的是( )
| A.H2O(g)====H2(g)+1/2O2(g) ΔH=+242 kJ·mol-1 |
| B.2H2(g)+O2(g) ====2H2O(l) ΔH=-484 kJ·mol-1 |
| C.H2(g)+1/2O2(g) ====H2O(g) ΔH=+242 kJ·mol-1 |
| D.2H2(g)+O2(g) ====2H2O(g) ΔH=+484 kJ·mol-1 |
下列反应中,反应产物的总焓大于反应物总焓的是()
| A.氢气在氧气中燃烧 | B.铁丝在氧气中燃烧 |
| C.硫在氧气中燃烧 | D.焦炭在高温下与水蒸气反应 |