研究下表信息可直接得出的结论是
| 元素 |
F |
Cl |
Br |
I |
| 氢化物组成 |
HF |
HCl |
HBr |
HI |
| 氢化物形成的难易程度 |
H2、F2混合,冷暗处剧烈化合并发生爆炸 |
H2、Cl2混合,光照或点燃时发生爆炸 |
H2、 Br2混合,加热时发生化合 |
H2、I2混合,加热化合,同时又分解 |
| 氢化物的热稳定性 |
很稳定 |
稳定 |
较稳定 |
较不稳定 |
A.同周期元素的金属性随原子序数递增而增强
B.同周期元素的非金属性随原子序数递增而增强
C.第ⅦA族元素的非金属性随电子层数的增加而减弱
D.第ⅦA族元素的金属性随电子层数增加而减弱
下列排列顺序正确的是()
①热稳定性HF>H2O>NH3 ②离子半径:Na+>Mg2+>F-
③酸性:盐酸>碳酸>醋酸④结合质子能力:OH->CO32->HCO3-
| A.①③ | B.②④ | C.①④ | D.②③ |
利用下列反应不能制得括号中纯净物质的是:
| A.乙烯与水加成(乙醇) |
| B.乙烯与氯气加成(1,2-二氯乙烷) |
| C.氯气与苯用氯化铁作催化剂反应(氯苯) |
| D.等物质的量的氯气与乙烷在光照条件下反应(氯乙烷) |
下列事实能用同一原理解释的是:
| A.SO2和Cl2都能用于漂白 |
| B.I2、NH4Cl晶体受热都逐渐消失 |
| C.配制Fe(NO3)3和Sn(NO3)2溶液均要加入稀硝酸 |
| D.SO2可使加酚酞的氢氧化钠溶液和酸性高锰酸钾溶液的红色都褪去 |
下表为周期表的一部分,有关短周期X、Y、Z、R四种元素叙述正确的是: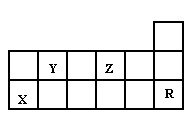
| A.热稳定性:Y的气态氢化物<Z的气态氢化物 |
| B.X的最高价氧化物对应水化物的酸性比Y的强 |
| C.X元素的单质能与所有强酸发生反应放出H2 |
| D.R元素的单质化学性质活泼 |
下列表示对应化学反应的离子方程式正确的是:
| A.玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH-=Na2SiO3↓+H2O |
| B.硫酸亚铁溶液被空气中氧气氧化:4Fe2+ +O2+4H+=4Fe3+ +2H2O |
| C.向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| D.用食醋和淀粉-KI试纸检验碘盐中的KIO3IO3-+5I-+6H+=3I2+3H2O |