NA表示阿伏加德罗常数,下列说法正确的是
| A.常温常压下,11.2 L氯气所含原子数目为NA |
B.2 L 0.2 mol / L K2SO4溶液 物质的量浓度为0.4 mol / L 物质的量浓度为0.4 mol / L |
| C.1 mol Na作还原剂可提供电子数为NA |
| D.同温、同压下NA个CO2分子和NA个O2分子的体积相同 |
美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200℃时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为:C2H5OH +3O2 =2CO2 +3H2O,电池示意如图,下列说法正确的是
| A.a极为电池的负极,乙醇被还原 |
| B.电池工作时电子由b极沿导线经灯泡再到a极 |
| C.电池正极的电极反应为:2H+ + O2 + 4e-= H2O |
| D.电池工作时1mol乙醇被氧化时,就有12mol质子 |
某温度下,H2(g) + CO2(g)  H2O(g) + CO(g)的平衡常数K = 9/4,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,其起始浓度如下表所示,下列判断不正确的是
H2O(g) + CO(g)的平衡常数K = 9/4,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,其起始浓度如下表所示,下列判断不正确的是
| 起始浓度 |
甲 |
乙 |
丙 |
| c(H2)/mol.L-1 |
0.010 |
0.020 |
0.020 |
| c(CO2)/mol.L-1 |
0.010 |
0.010 |
0.020 |
A.平衡时,乙中CO2的转化率大于60%,平衡常数也随之变大
B.平衡时,甲和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.008 mol/L
D.反应开始时,三个容器中,丙中的反应速率最快,甲中的反应速率最慢
如图甲为锌铜原电池装置,乙为电解熔融氯化钠装置。则下列说法正确的是
| A.甲装置中锌为负极,发生氧化反应,SO42-向铜极移动 |
| B.乙装置中B是氯气出口,A是钠出口 |
| C.乙装置中铁极为阳极,石墨为阴极 |
| D.甲装置中的反应是自发反应,有化学能转化为电能;乙装置中的反应是非自发反应,有电能转化为化学能 |
下列说法中,正确的是
A.对于2SO2(g)+O2(g) 2SO3(g) ΔH=-QkJ·mol-1(Q>0),若反应中充入1molSO2和足量的氧气反应时,放出的热量一定是Q/2 kJ 2SO3(g) ΔH=-QkJ·mol-1(Q>0),若反应中充入1molSO2和足量的氧气反应时,放出的热量一定是Q/2 kJ |
| B.热化学方程式中的化学计量数不能用分数表示 |
| C.Zn(s)+H2SO4(aq)==ZnSO4(aq)+H2(g) ΔH<0,该反应的化学能可以转化为电能 |
| D.ΔH的大小与热化学方程式的化学计量数无关 |
在恒容密闭容器中发生反应2NO2 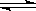 2NO+O2,下列所述可以说明反应达到平衡状态的是
2NO+O2,下列所述可以说明反应达到平衡状态的是
①单位时间内生成n molO2的同时生成2n molNO2
②单位时间内生成n molO2的同时生成2n molNO
③混合气体的颜色不再改变
④混合气体的密度不再改变
| A.①③ | B.②④ | C.①③④ | D.①②③④ |