已知NaHSO3溶液显酸性,溶液中存在以下平衡:
HSO3-+ H2O  H2SO3 + OH- ①
H2SO3 + OH- ①
HSO3- H+ + SO32- ②
H+ + SO32- ②
向0.1mol·L-1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是
| A.加入少量固体NaOH,平衡①左移,平衡②右移,溶液中c(HSO3-)增大 |
| B.加入等体积等浓度Na2SO3溶液,则3c(Na+) = 2[c(HSO3-) + c(H2SO3) +c(SO32-)] |
C.加入少量NaOH溶液, 、 、 的值均增大 的值均增大 |
| D.加入氨水至中性,则2c(Na+) = c(SO32-)>c(H+) = c(OH-) |
下列说法不正确的是:
| A.Ksp只与难溶电解质的性质和温度有关 |
| B.由于Ksp(ZnS)>Ksp(CuS),所以ZnS沉淀在一定条件下可转化为CuS沉淀 |
| C.其他条件不变,离子浓度改变时, Ksp不变 |
| D.两种难溶电解质作比较时, Ksp小的,溶解度一定小 |
准确量取25.00mLKMnO4溶液,可选用的仪器是:
| A.50mL量筒 | B.10mL量筒 |
| C.50mL酸式滴定管 | D.50mL碱式滴定管 |
25℃时,下列溶液中微粒存在情况合理的是
| A.Fe2+、Mg2+、ClO-、Cl-能大量共存 |
| B.含Br-、K+、Na+、HSO3-的溶液,通入SO2后这些离子仍能大量共存 |
C.含K+、Na+、NO3-、CH3COO-的溶液中c(H+)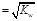 |
| D.硝酸钠和碘化钡混合溶液中,溶质离子浓度为c(Ba2+)=0.2mol·L-1,c(Na+)=0.2mol·L-1,c(NO3-)=0.3mol·L-1,c(I-)=0.1mol·L-1 |
根据下图,下列判断中正确的是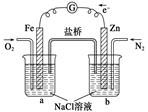
| A.烧杯a中的溶液pH升高 |
| B.烧杯a中发生的反应为2H2O+2e-=H2↑+2OH- |
| C.烧杯b中发生还原反应 |
| D.烧杯b中发生的反应为2Cl--2e-=Cl2↑ |
下列热化学方程式书写正确的是(ΔH的绝对值均正确)
A.C(s)+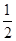 O2(g)=CO(g) ΔH=-110.5kJ·mol-1 (燃烧热) O2(g)=CO(g) ΔH=-110.5kJ·mol-1 (燃烧热) |
| B.2H2O(g)=2H2(g)+O2(g) ΔH=+483.6 kJ·mol-1(反应热) |
| C.C2H5OH+3O2=2CO2+3H2O ΔH=-1368.8 kJ·mol-1(反应热) |
| D.2NaOH(aq)+H2SO4(aq)=Na2SO4 (aq)+2H2O(l) ΔH=-114.6 kJ·mol-1(中和热) |