孔雀石主要含Cu2(OH)2CO3,还含少量FeO、SiO2。以孔雀石为原料可制备CuSO4·5H2O步骤如下:

(1)写出孔雀石与稀硫酸反应的化学方程式:___________。
(2)溶液A的金属离子有Cu2+、Fe2+。实验步骤中试剂①最佳选____(填代号)。
A.KMnO4 B.Cl2 C.H2O2 D.HNO3
(3)溶液B中加入CuO作用是______________。
(4)常温下Fe(OH)3的Ksp=1×10-39,若要将溶液中的Fe3+转化为Fe(OH)3沉淀,使溶液中c(Fe3+)降低至1×10—3mol/L,必需将溶液pH调节至____。
(5)由溶液C获得CuSO4·5H2O晶体,需要经_______、______和过滤。
(6)可用KMnO4标准溶液测定溶液A中Fe2+的浓度,量取A溶液20.00ml,用0.010mol/L酸性KMnO4标准溶液滴定,消耗KMnO4 10.00ml, A溶液中Fe2+的物质的量浓度____mol/L.(反应原理:MnO4- + 5Fe2++8H+=Mn2++5Fe3++4H2O)
(9分)某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振谱表明分子中只有一种类型的氢。
(1)A的结构简式为;
(2)A中的碳原子是否都处于同一平面?(填“是”或者“不是”);
(3)在下图中,D1、D2互为同分异构体,E1、E2互为同分异构体。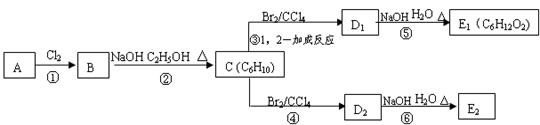
反应②的化学方程式为;
C的化学名称为;
E2的结构简式是;
④、⑥的反应类型依次是

近年来,乳酸CH3CH(OH)COOH成为人们的研究热点之一。乳酸可以用化学方法合成,也可以由淀粉通过生物发酵法制备。乳酸有许多用途,其中利用乳酸聚合而合成的高分子材料,具有很好的生物兼容性,它无论在哺乳动物体内或自然环境中,最终都能够降解成二氧化碳和水。请完成下列有关问题:
(1)乳酸在发生下列变化时所用的试剂①________________,②________________;
CH3CH(OH)COOH CH3CH(OH)COONa
CH3CH(OH)COONa CH3CH(ONa)COONa
CH3CH(ONa)COONa
(2)乳酸可以跟精制的铁粉反应制备一种补铁的药物,反应的化学方程式为
2CH3CH(OH)COOH+Fe [CH3CH(OH)COO]2Fe+H2↑
[CH3CH(OH)COO]2Fe+H2↑
该反应中氧化剂是________________,还原产物是________________。
(3)由乳酸可以制取 ,请写出设计合成实验时所涉及的有机反应类型:___________________。
,请写出设计合成实验时所涉及的有机反应类型:___________________。
(4)若碳原子以单键与四个不同的原子或原子团相结合,则称该碳原子为“手性碳原子”,含有手性碳原子的分子称为“手性分子”,手性分子往往具有一定生物活性。乳酸分子是手性分子,乳酸[③CH3②CH(OH)①COOH]的手性碳原子是________________号碳原子。
(1)下图是维生素A的分子结构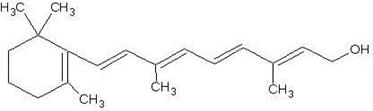
①维生素A中的官能团名称是,
②1mol维生素A最多能与mol溴反应。
③试指出维生素A可能发生的化学反应(写出反应类型,任写两种即可)
:
(2)系统命名:(CH3)2 C(OH)CH2CH3它的H-NMR谱中有个峰,此化合物在浓硫酸作用下发生消去反应,生成的有机产物的结构简式:
原子序数依次增大的四种主族元素A、B、C、D分别处于第一至第四周期,其中A原子核是一个质子;B原子核外电子有6种不同的运动状态,B与C可形成正四面体型分子,D原子外围电子排布为3d104s1。请回答下列问题:
(1)这四种元素中电负性最大的是 (填元素符号)、第一电离能最小的是 (填元素符号)
(2)C所在的主族元素气态氢化物中,沸点最低的是 (填化学式)
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体结构如右图所示,其原子的杂化类型为 ;
(4)D的水合醋酸盐晶体局部结构如右图,该晶体中含有的化学键是 (填选项序号);
①极性键 ②非极性键 ③配位键 ④金属键
有A、B、C、D、E五种短周期元素,其原子序数依次增大。A原子的电子层数与它的核外电子总数相同,B原子核外最外层电子数是次外层电子数的2倍,C元素的原子基态时2p能级是2s能级上的电子数的2倍,D是该周期中原子半径最大的主族元素,E原子的第一至第四电离能(kJ·mol-1)分别为:578、1817、2745、11575。请回答下列问题:
(1) C、D两元素形成的化合物的晶体类型是 。BC2的结构式
(2)若F是D的同主族下一周期元素,则F的电子排布式是:
(3)写出E的最高价氧化物对应的水化物与D的最高价氧化物对应的水化物反应的离子方程式 。
(4)A2C分子间因存在“氢键”的作用而彼此结合形成(A2C)n。在该分子形成的晶体中每个A2C分子被4个A2C分子包围形成变形的四面体,通过“氢键”相互连接成庞大的分子晶体,其结构示意图如右图所示,试填空。
①含1molA2C的该晶体中有_____mol“氢键”。
②若G是C的同主族下一周期元素,请比较A2C与A2G沸点的高低______________。