对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(1)含氰废水中的CN-有剧毒。
①CN-中C元素显+2价, N元素显-3价,用原子结构解释N元素显负价的原因是
②在微生物的作用下,CN-能够被氧气氧化成HCO3-,同时生成NH3,该反应的离子方程式为 。
(2)含乙酸钠和对氯酚(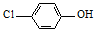 )的废水可以利用微生物电池除去,其原理如下图所示。
)的废水可以利用微生物电池除去,其原理如下图所示。
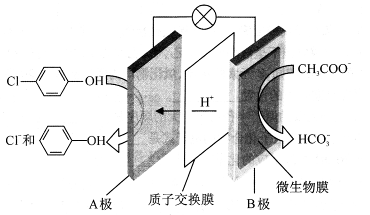
①B是电池的 极(填“正”或“负”);
②A极的电极反应式为 。
(3)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如下图所示(图中“HA”表示乳酸分子,A- 表示乳酸根离子)。

①阳极的电极反应式为
②简述浓缩室中得到浓乳酸的原理:
③电解过程中,采取一定措施可控制阳极室pH约为6-8,此时进入浓缩室的OH-可忽略不计。
400mL 10 g•L-1乳酸溶液通电一段时间后,浓度上升为145 g•L-1(溶液体积变化忽略不计),阴极上产生的H2在标准状况下的体积约为 L。(乳酸的摩尔质量为90 g• mol-1)
现有电解质溶液:①Na2CO3②NaHCO3③CH3COONa④ NaOH
(1)当四种溶液的pH相同时,其物质的量浓度由大到小的顺序是(填编号,以下相同)
(2)在上述四种电解质溶液中,分别加入AlCl3溶液,无气体产生的是
(1)纯水中c(H+)=5.0×10-7mol/L,则此时纯水中的c(OH-)=_______________;若温度不变,滴入稀硫酸使c(H+)=5.0×10-3mol/L,则c(OH-)=_______________;在该温度时,往水中滴入NaOH溶液,溶液中的C(OH-)=5.0×10-2 mol/L,则溶液中c(H+)= 。
某课外兴趣小组在进行“诚信商品”实验时,随机抽取市售“碳酸氢钠”样品(成分说明见右表所示)。经检验杂质只含NaCl,准确称取8.5g样品,加入100mL盐酸恰好完全反应生成2.24L气体(标准状况)。
试回答下列问题:
(1)样品中NaHCO3的物质的量;
(2)样品中小苏打的质量分数;
(3)所用盐酸的物质的量浓度;
(4)根据计算结果及成分说明所提供信息,此产品(填“可以”或“不可以”)列入“诚信商品”。
资料卡片:溴在水中溶解度不大(稀溴水呈黄色),易溶于CCl4等有机溶剂。
某校化学实验兴趣小组在“探究Cl2、Br2的氧化性”的系列实验中 发现:在足量的稀氯化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色。
发现:在足量的稀氯化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色。
(1)提出问题:Fe3+、Br2谁的氧化性更强?
(2)猜想:①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生氧化 还原反应所致,则溶液呈黄色是含(填化学式)所致。
还原反应所致,则溶液呈黄色是含(填化学式)所致。
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生氧化还原反应所致,则溶液呈黄色是含(填离子符号)所致。
(3)设计实验并验证:丙同学为验证乙同学的观点,利用下列 提供的试剂,设计出一种
提供的试剂,设计出一种 方案进行了实
方案进行了实 验,并通过观察现象,得出乙同学的观点正确。
验,并通过观察现象,得出乙同学的观点正确。
供选用的试剂:酚酞、CCl4、无水酒精、KSCN溶液、蒸馏水等。
请你写出丙同学选用的试剂是,实验中观察到的现象是。
(4)结论:氧化性:Br2>Fe3+
在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生反应的离子方程式是。
(5)实验后的思考:根据上述实验推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是(填离子符号)。
现有下列四种物质:Na2SO4、BaSO4、蔗糖(C12H22O11)、H2SO4,按照一定的依据,能找出一种物质与其它三种物质不同,从而分成两类。请你试试看,一共能找出多少种分法,把分类的依据和结果写在下面的表格中。(填三种即可)
| 与其它三种不同的物质 |
分类依据 |