CO不仅是家用煤气的主要成分,也是重要的化工原料。下图是用某些简单有机物在低温、低压和催化剂存在下合成具有优良性能的装饰性高分子涂料、黏胶剂的基本过程。
已知CaC 2 与水反应的化学方程为CaC 2 +2H 2 O  Ca(OH) 2 +HC≡CH↑。回答下列问题:
Ca(OH) 2 +HC≡CH↑。回答下列问题:
(1)写出G的结构简式。
(2)写出图中生成CH 3 OH(甲醇)的化学方程式。写出在浓硫酸作用下生成H的化学方程式。
(3)指出上述工艺的优点是什么?
为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了 加成反应。乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得的乙炔中还可能含有少量还原性的杂质气体,由此他提出必须先除去之,再与溴水反应。
请你回答下列问题:
(1)写出甲同学实验中两个主要的化学方程式、。
(2)甲同学设计的实验(填能或不能)验证乙炔与溴发生加成反应,其理由是
(a)使溴水褪色的反应,未必是加成反应
(b)使溴水褪色的反应,就是加成反应
(c)使溴水褪色的物质,未必是乙炔
(d)使溴水褪色的物质,就是乙炔
(3)乙同学推测此乙炔中必定含有的一种杂质气体是,它与溴水反应的化学方程式是;在验证过程中必须将此杂质全部除去。
(4)请你选用下列四个装置(可重复使用)来实现乙同学的实验方案,将它们的编号填入方框,并写出装置内所放的化学药品。

合成氨的流程示意图如下:
回答下列问题:
(1)工业合成氨的原料是氮气和氢气。氮气是从空气中分离出来的,通常使用的两种分离方法是____________、____________;氢气的来源是水和碳氢化合物,写出分别采用煤和天然气为原料制取氢气的化学方程式________________________,__________________________。
(2)设备A中含有电加热器,触媒和热交换器,设备A的名称是________,其中发生的化学反应方程式为__________________________。
(3)设备B的名称为________,其中m和n是两个通水口,入水口是________(填“m”或“n”)。不宜从相反方向通水的原因是________________________________________。
(4)设备C的作用是____________________________________________。
(5)在原料气制备过程中混有的CO对催化剂有毒害作用,欲除去原料气中的CO,可通过如下反应来实现:
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
已知1 000 K时该反应的平衡常数K=0.627,若要使CO的转化率超过90%,则起始物中c(H2O)∶c(CO)不低于________。
将下列家庭常用药物与相应作用连线。
板蓝根冲剂伤口消炎
甘草片退热止痛
红霉素抑制胃痛、助消化
扑尔敏抗菌消炎
阿司匹林治疗感冒
碘酒镇咳化痰
胃舒平抗过敏
在 中用虚线标示出氨基酸形成肽键时断裂化学键的位置。
中用虚线标示出氨基酸形成肽键时断裂化学键的位置。
乙醇汽油作为一种新型清洁燃料,是目前世界上可再生能源的发展重点,而且具有较好的经济效益和社会效益,终将成为汽油和柴油的替代品。
(1)写出乙醇完全燃烧的化学方程式:______________________________。
(2)乙醇燃烧时如果氧气不足,可能还有CO生成。用如图装置验证乙醇的燃烧产物中有CO、CO2、H2O,应将乙醇的燃烧产物依次通过(按气流从左到右的顺序填装置编号)________。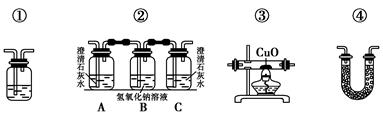
(3)实验时可观察到装置②中A瓶的石灰水变浑浊。A瓶溶液的作用是________;B瓶溶液的作用是________;C瓶溶液的作用是_________________________。
(4)装置③的作用是________;装置①中所盛的是________,作用是______________________。
(5)装置④中所盛的固体药品是________,它可以验证的产物是________。
(6)尾气应如何处理?_________。
(7)海底有大量的甲烷水合物。等质量的甲烷和乙醇完全燃烧产生温室气体CO2较多的是________。