铁及其化合物在工农业生产、环境保护等领域中有着重要的作用。
(1)酸性条件下,硫酸亚铁可将MnO2还原为MnSO4,该反应的离子方程式为:_____________。
(2)分析表明,铁在浓硫酸中发生钝化时,生成的氧化物中Fe、O两种元素的质量比为28∶11,则其化学式为______________。
(3)铁及其化合物可用于消除环境污染。常温下,硫酸亚铁能将SO2转化为SO42-,总反应为2SO2+O2+2H2O=2H2SO4,其中一个反应为4Fe2++O2+4H+=4Fe3++2H2O,则另一个反应的离子方程式为____________________。
常温下,用氧缺位铁酸锌ZnFe2Oy可以消除NOx污染,使NOx转变为N2,同时ZnFe2Oy转变为ZnFe2O4。若2 mol ZnFe2Oy与足量NO2反应可生成0.5 mol N2,则y=____________。
(4)工业上常采用如图所示电解装置,利用铁的化合物将气态废弃物中的硫化氢转化为可利用的硫。通电电解,然后通入H2S时发生反应的离子方程式为:2[Fe(CN)6]3-+2CO32-+H2S=2[Fe(CN)6]4-+2HCO3-+S↓。电解时,阳极的电极反应式为___________;电解过程中阴极区溶液的pH______________(填“变大”、“变小”或“不变”)。
(6分)将3 mol A和3 mol B混合于2 L的密闭容器中,发生如下反应:
3A(g)+B(g)  xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,C的平均反应速率为0.1 mol/(L·min)。试求:
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,C的平均反应速率为0.1 mol/(L·min)。试求:
(1)B的平均反应速率为。
(2)x的值为。
(3)5 min后,A、B的物质的量之比为。
(12分)已知烃A完全燃烧生成CO2和H2O的物质的量相等,且其相对分子质量小于30,F是高分子化合物,E是一种有香味的物质,E中碳原子数是D的两倍。A能发生以下转化: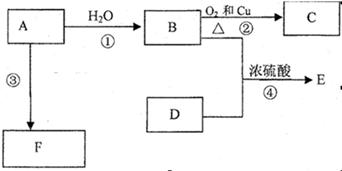
(1)A的电子式为:
(2)B中含官能团名称 ;D中含官能团名称;
(3)写出反应的化学方程式
②:反应类型:
③:反应类型:
④:反应类型:
(9分)A、X、Y、Z和W是原子序数依次增大的五种短周期元素。A和X可组成两种常温下为液态的化合物A2X、A2X2,X和Y也可组成两种常温下为固态的化合物Y2X、Y2X2,且Y2X、Y2X2的焰色反应均为黄色。在元素周期表中,A与Y同主族,X与Z同主族,Z与W相邻。请同答:
(1)A2X2的结构式,Y2X2的电子式。
(2)X、Z两种元素的氢化物中熔沸点较高的是(填化学式,下同);工业上将Z的低价氧化物转化为高价氧化物的化学方程式为。
(3)W元素在周期表中的位置为;实验室制备W单质的化学反应方程式为;在上述反应中氧化剂和还原剂的物质的量比为。
(13分)下图是元素周期表的一部分,表中的①—⑩中元素,用化学用语填空回答:
| 族 周期 |
I A |
IIA |
IIIA |
ⅣA |
VA |
ⅥA |
ⅦA |
0 |
| 二 |
① |
② |
③ |
|||||
| 三 |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|||
| 四 |
⑨ |
⑩ |
(1)在这些元素中,⑩原子的原子结构示意图为。
(2)写出①的最高价氧化物和②的单质的电子式,。
(3)用电子式表示③与④形成化合物的过程。
(4)①的单质和⑥的氧化物反应的化学方程式。
(5)写出⑤的单质与氢氧化钠反应的化学方程式:
写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式:。
(6)已知拆开l mol C—H键、l mol O=O键、l molC=O键、l mol H—O键分别需要吸收的能量为414kJ、498kJ、728kJ、464kJ。则l mol甲烷完全燃烧放出kJ的热量。
乙烯是石油化工最重要的基础原料,请根据以下框图回答:
41.以石油为原料的系列化工生产过程中,得到大量乙烯的主要方法是_______(选填序号)。
a. 水解 b. 分馏 c. 裂解 d. 裂化
42.有机物A俗称______________,含有的官能团名称是_________________.
43.B的分子式为C2H4O2,与纯碱反应能生成二氧化碳气体,写出反应A+B→C的化学
方程式___________________________________________________________(有机物用结构简式表示),该反应类型为______________________。