下列说法不正确的是
| A.Na与H2O的反应是熵增的放热反应,该反应能自发进行 |
| B.饱和Na2SO4溶液或浓硝酸均可使蛋白质溶液产生沉淀,但原理不同 |
| C.FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同 |
D.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s) Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液 Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液 |
甲酸和乙酸都是弱酸,当它们的浓度均为0.10 mol·L-1时,甲酸中的c(H+)约为乙酸中c(H+)的3倍。现有两种浓度不等的甲酸溶液a和b,以及0.10 mol·L-1的乙酸,经测定它们的pH从大到小依次为a、乙酸、b。由此可知
| A.a的浓度必小于乙酸的浓度 |
| B.a的浓度必大于乙酸的浓度 |
| C.b的浓度必小于乙酸的浓度 |
| D.b的浓度必大于乙酸的浓度 |
常温下,下列离子浓度的关系正确的是
| A.pH=2的盐酸与pH=12的氨水等体积混合:c(NH4+)=c(Cl-)>c(H+)=c(OH-) |
| B.0.2 mol·L-1的CH3COONa溶液与0.1 mol·L-1的HCl等体积混合:c(Na+)>c(Cl-)>c(CH3COO-)>c(H+)>c(OH-) |
| C.0.1 mol·L-1的HCN(弱酸)和0.1 mol·L-1的NaCN等体积混合:c(HCN)+c(CN-)+c(OH-)=c(Na+)+c(H+) |
| D.相同物质的量浓度时,溶液中c(NH4+)由大到小的顺序:NH4Al(SO4)2>NH4Cl>CH3COONH4>NH3·H2O |
室温时将浓度和体积分别为c1、V1的NaOH溶液和c2、V2的CH3COOH溶液相混合,下列关于该混合溶液的叙述错误的是
| A.若pH>7,则一定是c1V1=c2V2 |
| B.在任何情况下都是c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
| C.当pH=7时,若V1=V2,则一定是c1<c2 |
| D.若V1=V2、c1=c2,则c(CH3COO-)+c(CH3COOH)=c(Na+) |
已知温度T时水的离子积常数为KW,该温度下,将浓度为a mol· L-1的一元酸HA与b mol· L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
| A.a=b |
| B.混合溶液的pH=7 |
C.混合溶液中,[H+]=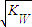 mol·L·-1 mol·L·-1 |
| D.混合溶液中,c(H+)+c(B+)===c(OH-)+c(A-) |
常温下,下列各组离子在指定溶液中能大量共存的是
| A.pH=1的溶液中:Fe2+、NO3-、SO42-、Na+ |
| B.由水电离的c(H+)=1×10-14 mol·L-1的溶液中:Ca2+、K+、Cl-、HCO3- |
| C.c(H+)/c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl- |
| D.c(Fe3+)=0.1 mol·L-1的溶液中:K+、ClO-、SO42-、SCN- |