黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。(1)冶炼铜的反应为8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号)。
(2)上述冶炼过程中产生大量SO2。下列处理方案合理的是 (填代号)。
a.高空排放 b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO3 d.用浓硫酸吸收
(3)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、Al2O3及不溶于强酸的SiO2)可制备Fe2O3。
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得。
据以上信息回答下列问题:
a.除去Al3+的离子方程式是 。
b.步骤②中滤液氧化的目的是 。
c.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为 。
证明炉渣中含有FeO的实验现象为 。
在氧化还原反应中,氧化剂______电子,发生的反应是_________反应;还原剂________电子,发生的反应是____________反应。氧化还原反应的实质是:___________。特征是:___________。如何来判断某个反应是否属于氧化还原反应:___________。
某河道两旁有甲乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、C1-、OH-、NO3-六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子、、。乙厂的废水中含有另外三种离子。对于该两厂的废水,可采取下列两种方法来处理。
(1)如果在废水中加一定量(选填:活性炭或铁粉),可以发生反应,离子方程式是,并且能够回收其中的金属(填写金属元素符号)。
(2)将甲厂和乙厂的废水按适当的比例混合,可以使废水中的某些离子转化为沉淀,写出两个离子方程式:;。经过滤后的废水主要含,可用来浇灌农田。
电解质是指在或下能够导电的。电解质导电的根本原因在于它在这种状态下能够出自由移动的离子。科学家从这个角度对化合物进行了分类,根据这种分类,酸、碱、盐应该属于。
丁达尔现象是区分胶体与溶液的一种最常用的方法。
(1)如图是在实验室中进行氢氧化铁胶体丁达尔现象实验的示意图,该图中有一处明显错误是___________,原因是_______________________(试从分散系的分类进行讨论说明)。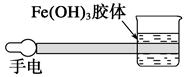
(2)欲在树林中观察到丁达尔效应,你认为一天中最有可能观察到该现象的时间是______,理由是__________。
(3)去树林观察丁达尔效应有诸多不便,聪明的你想出了许多在家里看到丁达尔效应的方法,其中最简单、最环保的方法是__________________________________。
按不同的分类方法,下列每组中都有一种物质与其他物质不同,试分析每组中物质的组成规律,将其中不同于其他物质的物质找出来。
(1)NaCl、KCl、NaClO、BaCl2________________。
(2)HClO3、KClO3、Cl2、NaClO3______________。
(3)H3PO4、H4SiO4、HCl、H2SO4_______________。
(4)空气、N2、HCl气体、CuSO4·5H2O_____________。
(5)铜、金、汞、钠____________________。