工业电解饱和食盐水模拟装置的结构如图所示:
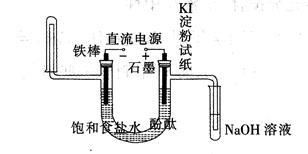
(1)写出电解饱和食盐水的化学方程式 ,该工业称为 工业
(2)实际生产中使用的盐往往含有一些杂质,在电解食盐水之前,需要提纯食盐水。为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作,正确的操作顺序是
①过滤 ②加过量的NaOH溶液 ③加适量的盐酸 ④加过量的Na2CO3溶液 ⑤加过量的BaCl2溶液
| A.①④②⑤③ | B.④①②⑤③ | C.②⑤④①③ | D.⑤②④③① |
(3)在该装置中写出装NaOH溶液试管中所发生的化学反应方程式(并用双线桥表示电子的转移的方向和数目) 。
(11分)在第3周期中,置换酸中氢的能力最强的元素的元素符号为,化学性质最稳定的元素符号是,最高价氧化物的水化物的酸性最强的化合物的化学式是,最高价氧化物的水化物的碱性最强的化合物的化学式是,显两性的氢氧化物的化学式是,该两性氢氧化物与盐酸、氢氧钠溶液分别反应的离子方程式为、,原子半径最大的金属元素的名称是,离子半径最小的离子结构示意图是。
(10分)2,3二氢呋喃是抗肿瘤药物的中间体,也用于电子化学品和香料的生产中,可由丙烯为原料合成: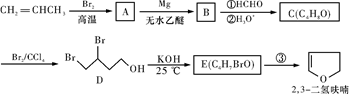
已知:①呋喃和四氢呋喃的结构简式分别为: 
②卤代烃 R—X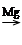 RMgX
RMgX RCOMgX
RCOMgX RCOH。
RCOH。
回答下列问题:
(1)呋喃、2,3二氢呋喃、四氢呋喃是否互为同系物? (填“是”或“否”)。
(2)用系统命名法命名化合物D: 。
(3)反应③的条件是________________。
(4)2,3二氢呋喃可转化为四氢呋喃,如何用简单的化学方法检验 2,3二氢呋喃是否完全转化? 。
(5)四氢呋喃还可由化合物C4H10O2在少量浓硫酸存在下制得,该反应的化学方程式为:____________。
(12分)有机物A(C10H20O2)有兰花香味,可用作香皂、洗发香波的芳香赋予剂。已知: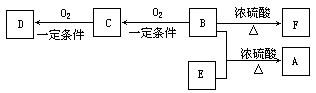
①B分子中没有支链;②D能与碳酸氢钠溶液反应放出二氧化碳;③D、E互为具有相同官能团的同分异构体,E分子烃基上的氢若被Cl取代,其一氯代物只有一种;④F可以使溴的四氯化碳溶液褪色。
(1)请写出A、D、F的结构简式 A: ;D: ;F: 。
(2)B可以发生的反应有 (填序号)。
①取代反应 ②消去反应 ③加聚反应 ④氧化反应
(3)D、F分子所含的官能团的名称依次是 、 。
(4)写出与D、E具有相同官能团的同分异构体的可能结构简式(任写一种):__________。
(10分)维生素C(又名抗坏血酸,分子式为C6H8O6)具有较强的还原性,放置在空气中易被氧化,其含量可通过在弱酸性溶液中用已知浓度的I2溶液进行滴定。该反应的化学方程式如下:
C6H8O6+I2===C6H6O6+2HI
现欲测定某样品中维生素C的含量,具体的步骤及测得的数据如下:
取10 mL 6 mol·L-1CH3COOH溶液,加入100 mL蒸馏水,将溶液加热煮沸后冷却。精确称取0.2000 g样品,溶解于上述冷却的溶液中,加入1 mL指示剂,立即用浓度为0.05000 mol·L-1的I2溶液进行滴定到终点,消耗21.00 mL I2溶液。
(1)实验中的指示剂是_____________。
(2)加入的CH3COOH稀溶液要先经煮沸、冷却后才能使用。煮沸的目的是________________;冷却的目的是__________________。
(3)计算样品中维生素C的质量分数(要求列式,且式中各物理量带单位)。
(8分)有机物A与乙酸无论以何种比例混合,只要总质量一定,完全燃烧后产生的水的质量也一定,试回答:
(1)若A与乙酸相对分子质量相等,且既能发生银镜反应又能发生酯化反应,则A的结构简式为 。
(2)若A由四种元素形成的两种官能团组成,相对分子质量与乙酸相等,且分子中氢原子都不与碳原子相连,则A的结构简式为 。
(3)若A分子中C、H元素质量分数之和为86.67%,其余为O,且A的相对分子质量小于200,则A的分子式为 。如果A分子中每个碳原子都达到饱和,且能与金属钠反应产生氢气,则A的结构简式为 。