(1)X是最简单的烯烃。现有如下的反应关系:(已知F是一种常见的塑料)

①X的结构简式为 ;C的官能团名称是 。
②由E制取F的化学方程式为 。
(2)某实验小组用下列装置进行A转化为B的实验。

①请写出A制取B的化学反应方程式:___________________________。
②甲和乙两个水浴作用不相同。甲的作用是_____________;乙的作用是_____________。
③试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,要除去该物质,可在混合液中加入___(填写字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
(3)阿斯匹林的结构简式为: ,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为 。
,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为 。
(4)某烃的分子式为C8H10,其不能使溴水褪色,但可使酸性KMnO4溶液褪色,且此烃与液溴在催化剂条件下只得到一种取代产物,其结构可能有 种。
| A.1种 | B.3种 | C.4种 | D.5种 |
苯丙醇胺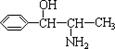 是一种人工合成的药品制剂,英文名称是Phenylpropanolamine,缩写为PPA,结构简式如图所示,其合成路线如下:
是一种人工合成的药品制剂,英文名称是Phenylpropanolamine,缩写为PPA,结构简式如图所示,其合成路线如下:
其中A~F分别代表一种有机化合物,合成路线中部分产物及反应条件已略去。已知: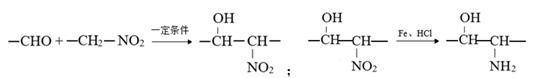
请回答下列问题:
(1)PPA的分子式是;F中官能团的名称是。
(2)E的结构简式是;烃A的核磁共振氢谱有种峰。
(3)上述合成路线中属于加成反应的是。(填数字序号)
(4)第②步的化学方程式是。
(5)E的一种同分异构体在一定条件下能发生缩聚反应,该反应的化学方程式是。
(16分)有机化工原料1,4-二苯基-1,3-丁二烯及某抗结肠炎药物有效成分的合成路线如下(部分反应略去试剂和条件):
已知:
Ⅰ. (R、R`表示烃基)
(R、R`表示烃基)
Ⅱ.
Ⅲ.



Ⅳ.




(1)抗结肠炎药物有效成分分子中的含氧官能团名称是。
(2)D的结构简式是_______________
(3)写出F与NaOH反应的化学方程式。
(4)下列说法正确的是________(填选项字母)。
| A.④的反应条件X和⑤的反应条件Y完全相同 |
| B.①②④⑤反应类型相同 |
| C.G不可以发生缩聚反应 |
| D.设计D→E和F→G两步反应的目的是防止酚羟基被氧化 |
(5)检验 有氯原子的方法是。
有氯原子的方法是。
(6)③的化学方程式是。
(7)1,4-二苯基-1,3-丁二烯有多种同分异构体,写出符合下列条件的同分异构体的结构简式:。
a.结构中有两个苯环,无其它环状结构
b.苯环上的一硝基取代产物有两种
c.其核磁共振氢谱有3种峰,峰面积之比为3∶2∶2
从有机物A开始有如图所示的转化关系(部分产物略去)。 A在NaOH溶液中水解生成B、C和D,1mol F与足量的新制Cu(OH)2碱性悬浊液加热充分反应可生成2mol红色沉淀。分析并回答问题: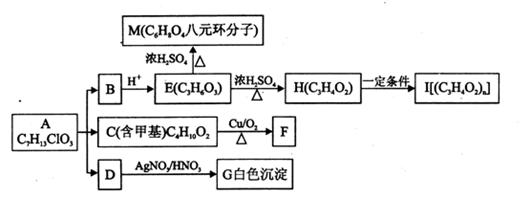
(1)A中含有的官能团有羟基、(填写官能团名称)
(2)C的名称(系统命名)是;E—H的反应类型是;M的核磁共振氢谱有组峰。
(3)C→F的化学方程式是。
(4)F与足量新制Cu(OH)2反应的化学方程式是。
(5)所有满足上述转化关系的A的结构简式是。
(6)E的某同系物甲(C4H8O3)有多种同分异构体,其中含有酯基和羟基,且水解产物不存在两个羟基连在同一个碳上的同分异构体有种。(不考虑立体异构)
选做(12分)【化学一有机化学基础】 聚谷氨酸(
聚谷氨酸( )是一种具有水溶性、可生物降解、可食用的对人体和环境无毒的高分子聚合物,广泛应用于食品和医药等领域。下图是根据实际需要和目的,对
)是一种具有水溶性、可生物降解、可食用的对人体和环境无毒的高分子聚合物,广泛应用于食品和医药等领域。下图是根据实际需要和目的,对 聚谷氨酸
聚谷氨酸 中的羧基进行化学修饰的路线,其中B、C、F均为高分子化合物。
中的羧基进行化学修饰的路线,其中B、C、F均为高分子化合物。
请回答:
(1)C的单体的结构简式为__________。D→E的反应类型是_________。
(2) 与NaHCO3溶液反应,可观察到的实验现象是_________。
与NaHCO3溶液反应,可观察到的实验现象是_________。
(3)下列关于CH3CH=CH2的说法中,正确的是__________(填字母序号)。
a.能使KMnO4酸性溶液褪色
b.它的同分异构体环丙烷属于不饱和烃
c.与HBr发生加成反应可得到两种产物
d.可以用溴的四氯化碳溶液鉴别丙烯和丙炔
(4)D的核磁共振氢谱有4个吸收峰,D发生银镜反应的化学方程式为:______________________。
(5)E与邻苯二甲酸 反应生成的产物DBP(C16H22O4)是广泛使用的增塑剂之一。DBP有多种同分异构体,其中符合下列条件的DBP的结构简式_____________________
反应生成的产物DBP(C16H22O4)是广泛使用的增塑剂之一。DBP有多种同分异构体,其中符合下列条件的DBP的结构简式_____________________
a.1mol化合物能与2molNaHCO3反应
b.苯环上只有两个相同的无支链取代基
c.苯环上的一氯取代物有三种
【化学一有机化学基础】有机物F的合成路线如图所示:
已知以下信息:
(1)RCOOR’ RCH2OH (2)
RCH2OH (2)
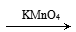
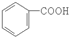
回答以下问题:
(1)A的结构简式为_____________________,G的结构简式为_____________________。
(2)B生成C的化学方程式为_____________________。
(3)检验E中含氧官能团的试剂是___________________,现象是___________________。
(4)E→F的反应类型是_____________________。
(5)写出A的一种符合下列条件的同分异构体的结构简式_____________________。
①属于芳香族化合物
②苯环上有四个取代基
③苯环上的一溴取代物只有一种