下列叙述不正确的是( )
① 熔点:金刚石>晶体硅>单质硫
② 气态氢化物的稳定性:H2O>HF>H2S
③ 同一主族元素的氢化物,相对分子质量越大,它的沸点一定越高
④ 因为常温下白磷可自燃,而氮气需要在放电时才与氧气反应,所以非金属性:P>N
⑤ 碱性氧化物一定是金属氧化物
| A.①②③ | B.②③④ | C.②④⑤ | D.①③⑤ |
 下列说法中不正确的是
下列说法中不正确的是
A.高吸水性树脂属于功能高分子材料
B.SiC、Al2O3的熔点很高,可用作高温结构陶瓷
C.光导纤维、合成纤维和人造纤维都是有机高分子化合物
D.合金拓展了金属材料的使用范围,合金中也可能含有非金属元素
下图是CO2电催化还原为CH4的工作原理示意图。下列说法不正确的是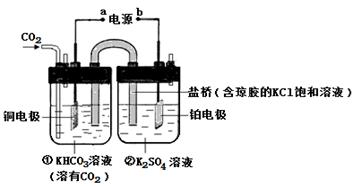
| A.该过程是电能转化为化学能的过程 |
| B.一段时间后,①池中n(KHCO3)不变 |
| C.一段时间后,②池中溶液的pH一定下降 |
| D.铜电极的电极反应式为CO2+8H++8e-=CH4+2H2O |
.把V L含有 和
和 的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为( )
的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为( )
A. 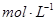 |
B. 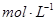 |
C. 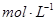 |
D. 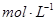 |
取一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有100 mL H2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10 mol/L的NaOH溶液, 产生沉淀的量与所加NaOH溶液的体积的关系如下图所示。则原H2SO4物质的量浓度是()
| A.1mol/L | B.2mol/L | C.3mol/L | D.4mol/L |
下列研究目的和示意图相符的是( )
| A |
B |
C |
D |
|
| 研 究 目 的 |
固定容积的密闭容器中,压强对反应: 2SO2(g)+O2(g)  2SO3(g)的影响 2SO3(g)的影响 |
固定容积的密闭容器中,温度对反应: N2(g) +3H2(g)  2NH3(g) ΔH< 0的影响 2NH3(g) ΔH< 0的影响 |
固定容积的密闭容器中,增大CO2浓度,对已达平衡的反应: CO(g)+H2O(g)  CO2(g)+H2(g)的影响 CO2(g)+H2(g)的影响 |
等质量Na、K 分别与足量水反应 |
| 示 意 图 |
 |
 |
 |
 |