下列说法正确的是
| A.增大反应物浓度可以增大活化分子百分数,从而使反应速率增大 |
| B.汽车尾气的催化转化装置可将尾气中的NO和CO等有害气体快速地转化为N2和CO2,其原因是催化剂可增大NO和CO反应的活化能 |
| C.在“反应热的测量实验”中测定反应后温度的操作方法:将量筒中的NaOH溶液经玻璃棒引流缓缓倒入盛有盐酸的简易量热计中,立即盖上盖板,并用环形玻璃搅拌棒不断搅拌,准确读出并记录反应体系的最高温度 |
| D.研制性能优良的催化剂既可以提高化学反应速率,又能起到很好的节能效果 |
下列实验装置正确,且能达到实验目的的是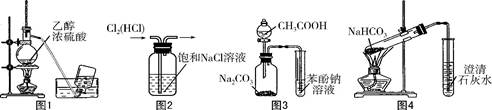
| A.利用图1装置制备乙烯 |
| B.利用图2装置除去Cl2中的HCl |
| C.利用图3装置证明酸性:CH3COOH>H2CO3>苯酚 |
| D.利用图4装置探究NaHCO3的热稳定性 |
设NA表示阿伏加德罗常数的值。下列说法正确的是
| A.一定条件下,0.2mol SO2与足量O2充分反应,生成SO3分子数为0.2NA |
| B.0.1mol—NH2(氨基)中含有的电子数为0.7NA |
| C.3.4g H2O2中含有的共用电子对数为0.1NA |
| D.常温常压下,16g O2和O3混合气体含有的氧原子数为NA |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.c(ClO-)=1.0mol·L-1的溶液中:Na+、SO32-、S2-、SO42- |
| B.常温下,C(H+)/C(OH— )=10-10的溶液中:Ca2+、Mg2+、HCO3-、I- |
| C.由水电离的c(H+)=1×10-12 mol·L-1的溶液中:Ba2+、K+、Cl-、NO3- |
| D.滴入少量KSCN溶液显红色的溶液中:Na+、K+、I-、SO42- |
下列有关物质的性质和应用不正确的是
| A.甲醛能使蛋白质变性,常用高浓度甲醛溶液浸泡食用海产品以防腐 |
| B.硅胶多乳、吸水能力强,常用作袋装食品的干燥剂 |
| C.过氧化钠能与二氧化碳反应产生氧气,可用作潜水艇的供氧剂 |
| D.锌的金属活泼性比铁强,可用于保护石油管道(碳素钢管)以减缓其腐蚀 |
下列有关化学用语表示正确的是
| A.明矾的化学式:KAl(SO4)2 |
B.氯离子的结构示意图: |
C.2 丙醇的结构简式:(CH3)2CHOH 丙醇的结构简式:(CH3)2CHOH |
D.溴化铵的电子式: |