下列热化学方程式正确的是
| A.2SO2+O22SO3;H =-196.6 kJ·mol-1 |
| B.H2 (g)+1/2O2 (g) = H2O(l);H =-285.8 kJ·mol-1 |
| C.2H2 (g)+O2 (g) = 2H2O(l);H =-571.6 kJ |
| D.C(s)+O2 (g) = CO2 (g);H = +393.5 kJ·mol-1 |
化学与生活密切相关,下列有关说法正确的是
| A.制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材 |
| B.铝的金属性较强,所以铝制容器在空气中容易被腐蚀 |
| C.“血液透析”利用了胶体的性质 |
| D.自行车钢架生锈主要是化学腐蚀所致 |
铬铁矿主要成分为FeO·Cr2O3,还含有杂质Al2O3。一般铬铁矿中Cr2O3质量分数约为40%。由铬铁矿制备重铬酸钾的方法如下: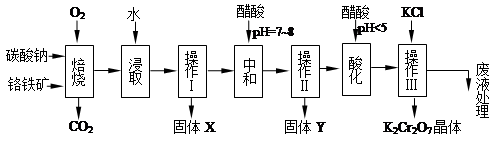
已知:
①4FeO·Cr2O3+8Na2CO3+7O2 8Na2CrO4+2 Fe2O3+8CO2↑;
8Na2CrO4+2 Fe2O3+8CO2↑;
②Na2CO3+Al2O3 2NaAlO2+CO2↑;
2NaAlO2+CO2↑;
③ Cr2O72-+H2O  2CrO42-+2H+
2CrO42-+2H+
根据题意回答下列问题:
(1)操作I为,固体X中主要含有(填写化学式);要检测酸化操作中溶液的pH是否等于4.5,应该使用(填写仪器或试剂名称)。
(2)酸化步骤用醋酸调节溶液pH<5,其目的是。
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、、过滤、、干燥。
(4)固体Y中主要含有氢氧化铝,请写出调节溶液的pH=7~8时生成氢氧化铝的离子方程式。
某无色溶液M可能含有离子OH-、HCO3-、CO32-、SO42-、SiO32-、AlO2-、NH4+、MnO4-、Cu2+、Mg2+、Na+、Fe3+中的若干种。取一定量的M溶液滴加盐酸,产生沉淀的物质的量与盐酸体积的关系如图所示。下列判断正确的是
| A.原溶液中可能含有NH4+、SO42- |
| B.最终溶液中最少含2种溶质 |
| C.原溶液中n(NaAlO2):n(Na2CO3)=1:1 |
| D.滴加盐酸初始阶段发生反应的离子方程式是:CO32-+H+=HCO3- |
归纳法是髙中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结:(均在常温下)
①pH=1的强酸溶液,加水稀释后,溶液中离子浓度都降低。
②pH=2的盐酸和pH=l的盐酸,C(H+)之比为2 :1
③pH相等的三种溶液:a.CH3COONa b.NaHCO3c.NaOH,其溶质物质的量浓度由小到大顺序为:c、b、a
④反应2A(s)+B (g)="2C" (g)+D (g)不能自发进行,则该反应△H一定大于0;
⑤已知醋酸电离平衡常数为Ka,醋酸根水解常数为Kb,水的离子积为Kw,则三者关系为:Ka•Kb=Kw
⑥若反应A(g)="2" B (g) 正反应的活化能为EakJ·mol-1,逆反应的活化能为EbkJ·mol-1,则△H=(Ea-Eb)kJ·mol-1
上述归纳正确的是
| A.全部 | B.③④⑤⑥ | C.②④⑤⑥ | D.①②④⑤ |
已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物稳定性大于Z的气态氢化物稳定性,X、Y为金属元素,X单质的还原性大于Y的单质的还原性。下列说法正确的是
| A.W与X形成的化合物中只含离子键 |
| B.W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 |
| C.X、Y、Z、W的原子半径依次减小 |
| D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |