某研究性学习小组同学对由NaHCO3和KHCO3组成的某均匀混合物进行实验,测得如下数据(盐酸的物质的量浓度相等)
| |
50mL盐酸 |
50mL盐酸 |
50mL盐酸 |
| m(混合物) |
9.2 g |
15.7 g |
27.6 g |
| V(CO2)(标况) |
2.24 L |
3.36 L |
3.36 L |
试计算:
(1)混合物与盐酸反应的的离子方程式 ;
(2)盐酸的物质的量浓度;
(3)混合物中两物质的物质的量之比。
(本题共8分)在密闭容器中进行X2(气)+ 3Y2(气) 2Z(气)的反应,其X2、Y2、Z的起始浓度依次为0.2mol/L、0.3mol/L、0.2mol/L,当反应达平衡时,浓度分别是a、b、c(mol/L),回答:
2Z(气)的反应,其X2、Y2、Z的起始浓度依次为0.2mol/L、0.3mol/L、0.2mol/L,当反应达平衡时,浓度分别是a、b、c(mol/L),回答:
①各物质的浓度有可能的是.
| A.c=0.5mol/L | B.b=0.5mol/L | C.c=0.4mol/L | D.a=0.3mol/L |
②若a=时,b=0.15mol/L。
③a、b的取值必须满足的一般条件是.
④a的取值范围是:.
在标准状况下,CO和CO2的混合气体15g所占的体积为11.2L,则;
(1)混合气体的摩尔质量是(2) CO和CO2两气体的体积比
某混合物是由NaCl、MgCl2、AlCl3三种物质组成的,Na、Mg、Al三种元素的质量比为23:12:9。求:(1)NaCl、MgCl2、AlCl3的物质的量的比?(2)氯原子为1mol时,混合物的质量?
配制250mL1.0mol/LH2SO4溶液,需用98%的浓硫酸溶液(ρ=1.84g/L)体积为多少?取25 mL1.0mol/LH2SO4溶液与锌反应,在标准状况下产生多少升H2?求硫酸锌的物质的量?
在300 mL 2 mol/L H2SO4溶液中,溶质的质量是?此溶液中含 H+的物质的量是?H+的物质的量浓度是?
其中含有个SO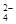 ? SO
? SO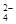 的物质的量浓度是?
的物质的量浓度是?