氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某小组模拟制备氨基甲酸铵的反应为:2NH3(g)+CO2(g) NH2COONH4(s) ΔH<0。(温度对反应的影响比较灵敏)
NH2COONH4(s) ΔH<0。(温度对反应的影响比较灵敏)
(1)如用下图装置和选用的试剂制取氨气,其中错误的是________;氨气的实验室制法的化学方程式是 。

(2)制备氨基甲酸铵的装置如下图所示,把NH3和CO2通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵的小晶体悬浮在CCl4中。 当悬浮物较多时,停止制备。(注:CCl4与液体石蜡均为惰性介质。)
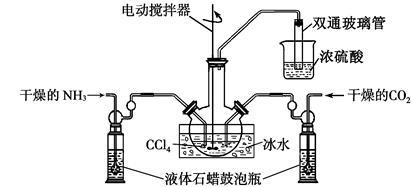
①发生器用冰水冷却的原因是 ;
液体石蜡鼓泡瓶的作用是 ;
双通玻璃管的作用是 ;
浓硫酸的作用是 。
②从反应后的混合物中分离出产品的实验方法是 (填写操作名称)。
为了得到干燥产品,应采取的方法是________(填写选项序号)。
a.常压加热烘干 b.高压加热烘干 c.减压40℃以下烘干
(3)制得的氨基甲酸铵可能含有碳酸氢铵、碳酸铵中的一种或两种。请利用下列试剂,设计实验方案,对制得的氨基甲酸铵中的杂质进行成分探究。
限选试剂:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸。
化学是一门以实验为基础科学。请根据下列仪器和实验装置回答有关问题:
(1)仪器②的名称是 。
(2)用①②③组合可制备CO2,写出实验室用此装置制备CO2的化学方程式 。
(3)收集CO2应选用装置 (填“④”或“⑤”)
(4)利用图⑥所示装置(集气瓶中预先装满CO2气体)来验证CO2的性质,先加入足量氢氧化钠溶液,观察到的现象是气球 (填“变大”、“变小”或“不变”),反应方程式为___________;再加入足量的盐酸,观察到的现象是气球 (填“变大”、“变小”或“不变”)。
利用图示仪器测量氧气体积,来测定高锰酸钾样品的纯度(杂质不参加反应)。实验步骤如下:
(1)检查气密性:连好发生装置后,将导管口的下端浸入水中, 。如果观察到导管口有气泡冒出,就证明装置不漏气。
(2)组装装置:连好的装置如图甲,其中有一处明显错误。在不移动、不调整酒精灯的前提下,需要调节 (选填字母)螺母改正错误。
(3)进行实验:采用正确的反应装置和图乙所示的收集装置制取并收集气体。下列说法正确的是 。;
A.加热时间过短,会使测量结果不准。
B.反应一段时间,排出反应装置内原有空气再连接乙装置收集气体,会使结果更准确。
实验小组研究碳酸钠和碳酸氢钠的性质。
实验一:甲、乙、丙三位同学分别用溶质质量分数为5%的NaHCO3溶液和Na2CO3溶液进行了如下实验。
| 实验内容 |
NaHCO3溶液 |
Na2CO3溶液 |
| (1)加入无色酚酞溶液 |
溶液变红 |
溶液变红 |
| (2)加入澄清石灰水 |
产生白色沉淀 |
现象Ⅰ |
| (3)加入5%的CaCl2溶液 |
产生白色沉淀、有气泡产生 |
产生白色沉淀 |
| (4)加入稀盐酸 |
现象Ⅱ |
有气泡产生 |
| (5)加热溶液,并用导管与澄清石灰水连接 |
石灰水变浑浊 |
石灰水无明显变化 |
(1)表中的现象Ⅰ为 ;用化学方程式表示现象Ⅱ的原因 。
(2)若要鉴别实验中用到的NaHCO3和Na2CO3两种溶液,实验一中提供了 种方法。
实验二:甲、乙、丙三位同学分别将各自实验一中NaHCO3溶液与澄清石灰水反应后的物质进行过滤,对滤液中的溶质成分进行了如下探究。
【查阅资料】
(1)氯化钙溶液显中性,与氢氧化钠溶液不反应。
(2)两种溶液的取用量不同,滤液中溶质的组成情况可能有:①NaOH;②Na2CO3;③NaOH和Ca(OH)2;④Na2CO3和NaHCO3;⑤Na2CO3和NaOH。
【进行实验】
| 实验操作 |
实验现象 |
实验结论 |
|
| 甲同学 |
取少量滤液于试管中,滴加足量的稀盐酸 |
有气泡产生 |
滤液中的溶质一定含有Na2CO3 |
| 乙同学 |
取少量滤液于试管中,向其中通入少量CO2 |
产生白色沉淀 |
则滤液中的溶质是 |
| 丙同学 |
取少量滤液于试管中,塞紧胶塞,并用导管与澄清石灰水连接,加热 |
澄清石灰水变浑浊 |
则滤液中的溶质是Na2CO3和NaHCO3 |
【反思与评价】
(1)根据丙同学的结论,NaHCO3溶液与澄清石灰水反应的化学方程式是 。
(2)甲同学进一步实验,确定了滤液中的溶质是Na2CO3和NaOH。其实验方案是 。
工业废水中含有硫酸亚铁、硫酸铜和污泥。某同学设计了利用废水制备硫酸亚铁晶体(FeSO4·7H2O)并回收铜的实验方案,流程如下:
已知:硫酸亚铁晶体受热易分解。
回答下列问题:
(1)步骤②中需加入的物质及目的是 。
(2)步骤③中发生反应的化学方程式为 。
(3)步骤④的操作是蒸发浓缩、降温结晶、 。
利用下图所示装置研究以下问题。
(1)利用图1研究燃烧的条件
水槽中放一定量热水,水面下a处放一小块白磷,观察到白磷不燃烧。在乙中放入二氧化锰和过氧化氢溶液,立即将甲倒扣在乙上,观察到甲中水面下降,白磷露出水面, 。通过对比实验研究了燃烧的一个条件,它是 。
(2)利用图2研究二氧化碳与氢氧化钠能反应,并检验反应后所得溶液中溶质的成分。
已知:氯化钙溶液呈中性,能与碳酸钠溶液发生复分解反应。
①A溶液是 。
②为达到上述实验目的,应进行的操作是:先打开 。通过观察现象,得出结论。