在人类社会的发展进程中,金属起着重要的作用。
(1)以下有关金属单质的叙述正确的是。
A.金属钠非常活泼,在实验室中保存在石蜡油或煤油中
B.用坩埚钳夹住一小块铝箔,在酒精灯上加热,可观察到铝箔熔化,并有熔融物滴下
C.铁单质与水蒸气反应的化学方程式为:2Fe+3H2O(g) Fe2O3+3H2
Fe2O3+3H2
(2)把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得浊液中逐渐加入1.00mol/LHCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示。
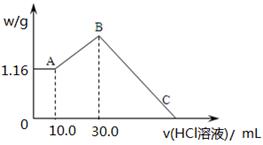
①A点的沉淀物的化学式为 。
②写出A点至B点发生反应的离子方程式: 。
③某溶液中溶有MgCl2和AlCl3两种溶质,若把两者分开,应选用的试剂为: 。
④原混合物中NaOH的质量是 g,C点(此时沉淀恰好完全溶解)HCl溶液的
体积为 mL。
(一)、将2 mol SO2和1 mol O2气体在1L的容器中混合,在一定条件下发生如下反应:2SO2(g)+O2 (g)  2SO3 (g)。若经过2s后测得SO3的浓度为0.6 mol/ L。试计算:(1)O2的化学反应速率V(O2)=; (2)2s时的O2浓度。
2SO3 (g)。若经过2s后测得SO3的浓度为0.6 mol/ L。试计算:(1)O2的化学反应速率V(O2)=; (2)2s时的O2浓度。
(二)、某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如下图所示。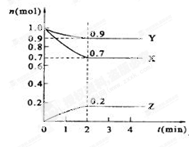
(1)X的转化率是
(2)由图中所给数据进行分析,该反应的化学方程式为;
(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=;
(4)当反应进行到第min,该反应达到平衡。
同学们已经学习了几种典型的有机化学反应类型——取代反应、加成反应,请写出下列反应的化学方程式,并判断其反应类型。
(1)由甲烷制取CH3Cl:_________________________________,属于________反应。
(2)由苯制取硝基苯:__________________________________,属于________反应。
(3)由苯制取环己烷:__________________________________,属于________反应。
电解原理在工业中有广泛应用。右图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题: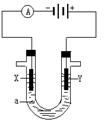
(1)若X、Y是惰性电极,a是200mLNaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,则电解池中X极上的电极反应为_____,在X极附近观察到的现象是 :_______。Y电极上的电极反应式是_________,检验该电极反应产物的方法是 :________________。当外电路通过0.02 mol电子时,充分混合电解后的溶液,忽略溶液体积变化,理论上溶液的PH值为_______。
(2)如果用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是_________,Y电极的材料是______,Y电极反应式是_______________。
已知电极材料:铁.铜.银.石墨.锌.铝,电解质溶液:氯化铜溶液.硫酸铁溶液.盐酸。按要求回答下列问题:
(1)电工操作上规定:不能把铜导线和铝导线连接在一起使用,请说明原因。__________。
(2)若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线构成原电池,请写出电极反应式,负极,正极。
(3)若总反应为:Cu+2H+= Cu2++H2,判断该装置属于原电池还是电解池?____。画出对应的装置图,标出电极材料和电解质溶液。_____
有甲、乙两种物质: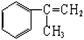
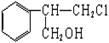
甲乙
(1)乙中含有的官能团的名称为____________________(不包括苯环)。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):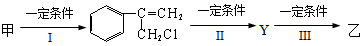
其中反应I的反应类型是___________,反应II的条件是_______________,反应III的化学方程式为___________________________________(不需注明反应条件)。
(3)下列物质不能与乙反应的是(选填序号)。
a.金属钠 b.溴水 c.碳酸钠溶液 d.氢氧化钠溶液
(4)乙有多种同分异构体,任写其中一种能同时满足下列条件的同分异构体结构简式。
a.苯环上的一氯代物有两种 b.遇FeCl3溶液显示紫色