下列溶液中粒子的物质的量浓度关系一定正确的是( )
A.常温下,pH=9的NaHA溶液:c(Na+)>c(HA-)>c(A2-)>c(H2A)
B.Na2CO3溶液:c(H+)-c(OH-)=c(HCO3-)+2c(CO32-)-c(Na+)
C.向NaOH溶液中滴入HCOOH溶液后溶液显碱性:c(HCOO-)>c(OH-)>c(H+)
D.浓度均为0.1 mol·L-1的HF溶液与KF溶液等体积混合:c(F-)+c(HF)=0.2 mol·L
自来水常用氯气进行消毒。如果在实验室用自来水配制下列物质的溶液,不会产生明显药品变质问题的是
| A.AgNO3 | B.NaI | C.NaOH | D.AlCl3 |
下列关于新制氯水及久置氯水的说法,不正确的是
| A.新制的氯水呈黄绿色,久置的氯水无色 |
| B.新制的氯水漂白作用强,而久置的氯水漂白作用很弱 |
| C.新制的氯水所含成分的种类多,而久置的氯水所含成分的种类较少 |
| D.新制的氯水中无氯离子,而久置的氯水中则含氯离子 |
在抗震救灾中要用大量漂白粉和漂白液杀菌消毒,下列说法中正确的是
| A.漂白粉是纯净物,漂白液是混合物 |
B.漂白粉的有效成分是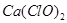 、CaCl2 、CaCl2 |
| C.工业上将氯气通入澄清石灰水制取漂白粉 |
| D.漂白粉使用时要让衣物浸泡一段时间是为了让漂白粉与气中的二氧化碳充分反应生成次氯酸 |
设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.标准状况下,1mol水的体积约为22.4L |
| B.3.4gOH-中含有的电子的数目为0.2NA |
| C.标准状况下,11.2 LCO2和SO2混合气体中含NA个氧原子 |
| D.1mol氖气和1mol氧气体积相同 |
下列气体所含分子数最少的是
| A.9.0g C2H6 | B.标准状况下5.6L 空气 |
| C.0.75mol N2 | D.3.01×1023个臭氧分子 |