25℃时,部分物质的电离常数如表所示:
请回答下列问题:
(1)同浓度的a.CH3COO-,b.HCO3-,c.CO32-,d.ClO﹣结合H+的能力由强到弱的顺序为__________(填编号)。
(2)向NaClO溶液中通入少量的CO2,反应的离子方程式为__________。
(3)pH相同的下列四种物质的溶液:a.Na2CO3,b.NaClO,c.CH3COONa,d.NaHCO3,物质的量浓度由大到小的顺序是__________(填编号)。
(4)常温下0.1mol•L﹣1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是__________(填序号)。
| A.c(H+) | B.c(H+)/c(CH3COOH) |
| C.c(H+)•c(OH﹣) | D.c(H+)•c(CH3COO﹣)/c(CH3COOH) |
若该溶液升高温度,上述5种表达式的数据增大的是__________。
(5)体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则HX的电离常数______(填“大于”、“等于”或“小于”)醋酸的电离常数;稀释后,HX溶液中由水电离出来的c(H+)_____(填“大于”、“等于”或“小于”)醋酸溶液中由水电离出来的c(H+)。
下列叙述正确的是______________。
①SO2、NO、NO2都是形成酸雨的因素,都能和水反应生成酸
②除去CO2中少量的SO2,将混合气体通过饱和Na2CO3溶液
③水晶的主要成分是SiO2
④SiO2与CO2都属于酸性氧化物,都不能与酸反应
⑤将CO2通入饱和Na2CO3溶液中有沉淀产生,继续通入CO2沉淀溶解
⑥某酸雨样本采集后放置一段时间,pH由4.68变为4.28,是因为水中溶解了较多的CO2
⑦CO2不能与CaCl2溶液反应,SO2也不能与CaCl2溶液反应
⑧实验室可用NaOH溶液处理NO2和SO2废气
⑨用稀双氧水清洗伤口可以杀菌消毒
⑩NO只能用排水集气法收集,不能用排空气法收集;而NO2只能用排空气法收集,不能用排水集气法
纯碱、烧碱等是重要的化工原料。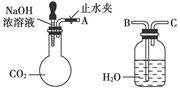
(1)利用上图所示装置可间接证明二氧化碳与烧碱溶液发生了反应。将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是,若其他操作不变,将A与C连接,可观察到的现象是。
(2)向NaOH溶液中通入一定量CO2,结晶后得到白色固体,该白色固体的组成可能是
| A.NaOH和Na2CO3; | |
| B.; | |
| C.; | D.。 |
(3)设计实验确定(2)中白色固体中存在A项中的阴离子:
| 实验操作 |
实验现象 |
结论 |
| (1)取少量白色固体于试管中,加足量水溶解,再加足量BaCl2溶液 |
||
| (2) |
用大试管收集一试管NO2气体,倒扣在盛水的水槽里,试管内产生的现象为;再往试管里通入适量氧气,试管内又产生的现象为。产生上述现象的原因是
工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是__________ ______________________________________。
(2)另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。写出生成Fe2+所有可能的离子反应方程式:。
若要确认其中有Fe2+,应选用(选填序号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.浓氨水 d.酸性KMnO4溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应的化学方程式为:。
然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中SO2的体积分数为。
已知有以下物质相互转化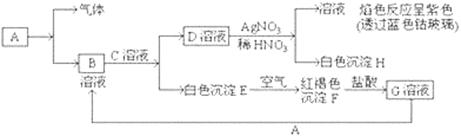
试回答:(1)写出E的化学式,H的化学式。
(2)写出由E转变成F的化学方程式。
(3)检验G溶液中的金属阳离子的方法是:;
向G溶液加入A的有关离子反应方程式。
(4)写出A在一定条件下与水反应的化学方程式。