一定条件下,通过下列反应可实现燃煤烟气中硫的回收,其中Y是单质。 SO2(g) + 2CO(g) 2X(g)+Y(l),为了测定在某种催化剂作用下的反应速率,在某温度下用超灵敏气体传感器测得不同时间的SO2和CO浓度如下表:
2X(g)+Y(l),为了测定在某种催化剂作用下的反应速率,在某温度下用超灵敏气体传感器测得不同时间的SO2和CO浓度如下表:
| 时间/s |
0 |
1 |
2 |
3 |
4 |
| c(SO2)/mol·L-1 |
1.00 |
0.50 |
0.23 |
3.00×10-37 |
3.00×10-37 |
| c(CO)/mol·L-1 |
4.00 |
3.00 |
2.46 |
2.00 |
2.00 |
下列说法不正确的是
A.X的化学式为CO2
B.前1s内v(X)=" 1.00" mol·L-1·s-1
C.该回收原理运用了SO2的还原性
D.该温度下,此反应的平衡常数的数值是3.33×1036
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略了净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )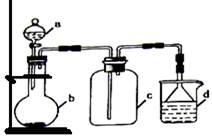
| 选项 |
a中的物质 |
b中的物质 |
c中收集的气体 |
d中的物质 |
| A |
氯化铵 |
NaOH |
NH3 |
H2O |
| B |
浓硫酸 |
Na2SO3 |
SO2 |
NaOH溶液 |
| C |
稀硝酸 |
Cu |
NO2 |
H2O |
| D |
浓盐酸 |
MnO2 |
Cl2 |
NaOH溶液 |
一定量的锌与100 mL 18.5 mol/L的浓硫酸充分反应后,锌完全溶解,同时生成气体甲 33.6 L(标准状况)。将反应后的溶液稀释至1 L,测得溶液中c(H+)="0.1" mol/L,则下列叙述中错误的是( )
| A.气体甲为SO2和H2的混合物 | B.气体甲中SO2与H2的体积之比为4:1 |
| C.反应中共消耗97.5 g Zn | D.反应中共转移3 mol电子 |
下列关于反应热的叙述,正确的是( )
| A.吸热反应一定要高温才能发生 |
| B.1mol酸与碱恰好中和时所放出的热量叫中和热 |
| C.已知C(s,石墨)=C(s,金刚石) △H=+1.9 kJ/mol,则石墨比金刚石稳定 |
| D.已知2H2(g)+O2(g)=2H2O(g) △H= —483.6 kJ/mol,则氢气的燃烧热为241.8 kJ |
下列反应既是氧化还原反应又是放热反应的是()
| A.过氧化钠与水反应 | B.氨水与稀硫酸的反应 |
| C.灼热的炭与CO2反应 | D.Ba(OH)2·8H2O与NH4Cl 的反应 |
下列有关说法正确的是( )
| A.大多数金属在自然界以游离态形式存在 |
| B.工业上,一般用热还原法获得Hg和Ag |
| C.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 |
| D.人们常用钢作建造材料而不用纯铁主要原因是钢的机械性能更好 |