下列叙述错误的是
| A.NaHCO3溶液中:c(H+) +c(H2CO3)=c(CO32-) +c(OH-) |
| B.25℃时,0.2mol·L-1盐酸与等体积0.05 mol·L-1Ba(OH)2溶液混合后,溶液的pH=1 |
| C.pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液中:2c(R2-)+c(HR-)=c(Na+) |
| D.25℃时,若0.3 mol·L-1 HY溶液与0.3 mol·L-1 NaOH溶液等体积混合后,溶液的pH=9,则: |
c(OH- )-c(HY)=c(H+)=1×10-9 mol·L-1
NH3可消除NO的污染,反应方程式为:6NO+4NH3=5N2+6H2O。现有NO与NH3的混合物共1 mol充分反应,若还原产物比氧化产物多1.4g,则下列判断中正确的是()
| A.原混合物中NO与NH3的物质的量之比可能为3:2 |
| B.有0.6 mol NH3被氧化 |
| C.生成还原产物2.8g |
| D.原混合气体中含氨气为0.2 mol或0.7 mol |
常温下,含a mol CH3COOH和b mol NaOH的两溶液混合后,下列推论不正确的是( )
| A.若a≤b,则混合溶液的pH大于7 |
| B.若a=2b,溶液呈酸性,则[CH3COO-]>[Na+]>[CH3COOH]>[H+]>[OH-] |
| C.混合溶液中[Na+]+[H+]=[OH-]+[CH3COO-] 一定成立 |
| D.混合溶液中[CH3COO-]+[CH3COOH]=a mol/L 一定成立 |
向某恒容密闭容器中充入一定量CO2和H2,发生反应:CO2(g)+H2(g) HCOOH(g)
HCOOH(g)
测得平衡体系中CO2的百分含量(CO2%)与反应温度变化的关系如图所示。下列物理量中,a点大于b点的是 ①正反应速率②逆反应速率③HCOOH(g)的浓度④对应温度时的平衡常数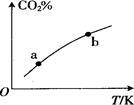
| A.①② | B.①③ | C.②④ | D.③④ |
用下列实验装置进行相应实验,能达到实验目的是()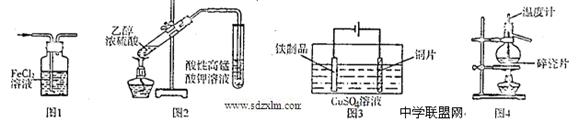
| A.用图1所示装置除去HCl气体中的少量C12 |
| B.用图2所示装置检验加热时产生的乙烯 |
| C.用图3所示装置在铁制品表面镀铜 |
| D.用图4所示装置分离溴的四氯化碳溶液 |
下列离子或分子在指定的分散系中一定能够大量共存的是()
| A.c(H+)=10-13 mol/L的溶液中:NO3-、SO42-、K+、Na+ |
| B.含Fe3+的溶液中中: Na+、K+、CH3COO-、HCO3- |
| C.铁与过量稀硫酸反应后的溶液中:[Al(OH)4]-、NH4+、Cl-、NO3- |
| D.空气中:SO2、NO、N2、NH3 |