常温下,1.0mol/L一元酸HA与等体积等浓度KOH溶液混合,所得溶液粒子的浓度关系如右表(不含水分子的5种粒子,A为短周期元素),下列说法正确的是
| 粒子 |
K+ |
A- |
X |
Y |
Z |
| 浓度(mol/L) |
0.50 |
0.49 |
c(X)>c(Y)>c(Z) |
A.元素A最高价氧化物对应水化物为HAO4
B.表格中X表示HA,Y表示H+
C.所得溶液中c(X)+ c(A-)= c(K+)
D.等体积等浓度的HA和盐酸分别加水稀释10倍后,pH (HA) >pH(HCl)
化学平衡常数(K)、电离常数(Ka、Kb)、溶度积常数(Ksp)等常数是表示、判断物质性质的重要常数,下列关于这些常数的说法中,正确的是
| A.化学平衡常数的大小与温度、浓度、压强有关,与催化剂无关 |
| B.Ka(HCN)<Ka(CH3COOH)说明相同物质的量浓度时,氢氰酸的酸性比醋酸强 |
| C.向氯化钡溶液中加入同浓度的碳酸钠和硫酸钠溶液,先产生BaSO4沉淀,则Ksp(BaSO4)>Ksp(BaCO3) |
| D.当温度升高时,弱酸、弱碱的电离常数(Ka、Kb)变大 |
已知FeS与某浓度的HNO3反应时生成Fe(NO3)3、H2SO4和某一单一的还原产物,若FeS和参与反应的HNO3的物质的量之比为1︰6,则该反应的还原产物是
| A.NO | B.NO2 | C.N2O | D.NH4NO3 |
下列有关化学用语,正确的是
| A.氧化亚铁溶于足量的稀硝酸中:FeO+2H+ = Fe2++H2O |
| B.向Ca(HCO3)2溶液加少量氢氧化钠溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
| C.少量CO2通入苯酚钠溶液中:C6H5O-+CO2+H2O=C6H5OH+HCO3- |
| D.醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘低。 
下列说法正确的是
| A.液滴中的Cl―由a区向b区迁移 |
B.液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e- 4OH- 4OH- |
| C.液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH―形成Fe(OH)2,进一步氧化、脱水形成铁锈 |
D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为:Cu-2e- Cu2+ Cu2+ |
下列说法正确的是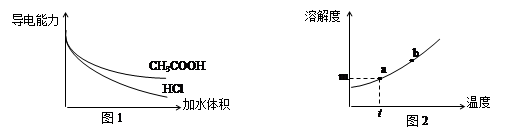
| A.图1表示pH相同的盐酸和醋酸加水稀释时溶液导电能力的变化 |
| B.图1表示物质的量浓度相同的盐酸和醋酸加水稀释时溶液导电能力的变化 |
| C.图2中,t ℃时饱和溶液的质量分数为m% |
| D.图2中,若保持温度不变,可以通过增加溶质的方法使溶液从a点变为b点 |