物质的性质决定了物质的用途,下面列出了金属的几种性质:①导热性、②导电性、③还原性、④延展性、⑤具有金属光泽。请在下面金属用途后的横线上填上金属性质对应的序号。
(1)用铝定制成包装用的铝箔 ;
(2)用铝制成的高压铝锅 ;
(3)用铁粉回收照相业废液中的银 ;
(4)电信业中大量使用的铜丝、金属电缆 。
有机物A的分子式为C3H8O,它能氧化成B,也能与浓H2SO4共热生成C。 若B不能发生银镜反应,C不能使溴水褪色,分别写出A、B、C的结构简式
下列各有机化合物都有多种官能团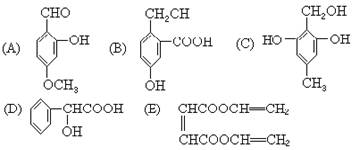
①可看作醇类的是____________________________
②可看作酚类的是____________________________
③可看作羧酸类的是__________________________
④可看作酯类的是____________________________
有机化学中取代反应的范畴很广。下列6个反应中,属于取代反应范畴的是(填写相应的字母):
簸箩酯是一种具有菠萝气味的食用香料,是化合物甲与苯氧乙酸 -O-CH2-COOH发生酯化反应的产物。
-O-CH2-COOH发生酯化反应的产物。
(1)甲一定含有的官能团的名称是_________。(1分)
(2)5.8g甲完全燃烧可产生0.3molCO2和0.3molH2O,甲蒸气对氢气的相对密度是29,甲分子中不含甲基,且为链状结构,其结构简式是______________________。(2分)
(3)苯氧乙酸有多种类型的同分异构体,其中能与FeCl3溶液发生显色反应,且有2种一硝基取代物的同分异构体是(写出任意2种的结构简式)___________ _____________。(每个1分,共2分)
(4)已知: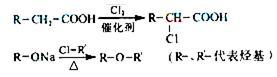
簸箩酯的合成线路如下: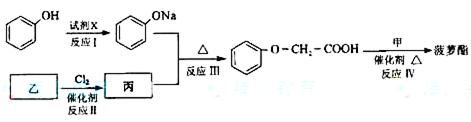
①及时X不可选用的是(选填字母)__________。(2分)
a、CH3COONa溶液 b、NaOH溶液 c、NaHCO3溶液 d、Na
②丙的结构简式是______________(2分),反应Ⅱ的反应类型是_______(1分)。
③反应Ⅳ的化学方程式是_________________________________________________。(2分)
某学生为了验证苯酚、醋酸、碳酸的酸性强弱,设计了如下实验装置: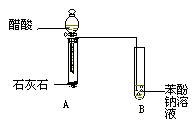
请回答下列问题
(1)仪器B中的实验现象 。
(2)仪器B中的化学方程式是 。
(3)该实验设计不严密,请改正 。