利用CO和H2在催化剂的作用下合成甲醇,发生的反应如下:CO(g)+2H2(g) CH3OH(g)。在体积一定的密闭容器中按物质的量之比1︰2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是
CH3OH(g)。在体积一定的密闭容器中按物质的量之比1︰2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是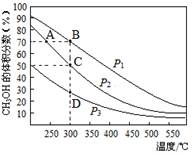
A.该反应的△H<0,且p1<p2
B.反应速率:ν逆(状态A)>ν逆(状态B)
C.在C点时,CO转化率为75%
D.在恒温恒压条件下向密闭容器中充入不同量的CH3OH,达平衡时CH3OH的体积分数也不同
反应A(g)+3B(g) 2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是
2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是
A.υ(D)="0.4" mol ·L-1·s-1B.υ(C)="0.5" mol ·L-1·s-1
C.υ(B)="0.6" mol ·L-1·s-1D.υ(A)="0.15" mol ·L-1·s-1
下列变化过程中,△S<0的是
| A.氯化钠溶于水中 | B.NH3(g)与HCl(g)反应生成 NH4Cl(s) |
| C.干冰(CO2)的升华 | D.CaCO3(s)分解为CaO(s)和CO2(g) |
在中和热测定的实验中不需要用到的仪器是
| A.量筒 | B.温度计 | C.环形玻璃搅拌棒 | D.天平 |
下列说法正确的是
| A.凡是自发反应都是放热的 | B.铁在潮湿空气中生锈是自发过程 |
| C.△S>0的反应在任何条件下都能自发进行 | D.电解池的反应是属于自发反应 |
下列物质属于强电解质的是
| A.CH3COOH | B.Cl2 | C.NH4Cl | D.SO2 |