乙酰苯胺为无色晶体,有“退热冰”之称。其制备原理为:

已知:①苯胺易被氧化;②苯胺、醋酸和乙酰苯胺的部分物理性质如下表:
| 试剂名称 |
熔点℃ |
沸点℃ |
溶解度(20 ℃) |
| 苯胺 |
-6.2 |
184.4 |
稍溶于水(3.4g),与乙醇、乙醚、苯混溶 |
| 乙酸 |
16.7 |
118 |
易溶于水、乙醇、乙醚等 |
| 乙酰苯胺 |
114~116 |
280~290 |
0.46g |
制备乙酰苯胺的实验步骤如下:
步骤1:在下图1装置的圆底烧瓶中,加入6.0 mL苯胺、9.0 mL冰醋酸及0.2g锌粉。
步骤2:控制温度计示数约105 ℃,小火加热回流1 h。
步骤3:趁热将反应混合物倒入盛有100 mL冷水的烧杯中,抽滤,洗涤,得到粗产品。
步骤4:通过重结晶提纯粗产品后,获得无色片状晶体,干燥后得目标产品。

图1 图2
(1)仪器a的名称为 。
(2)步骤1中加入锌粉的作用是 。
(3)步骤2中控制温度计示数约105 ℃的原因是 。
(4)步骤3中,抽滤装置如图2所示,仪器c的名称是 ,当过滤的溶液具有强酸性、强碱性或强氧化性时要用 代替布氏漏斗,停止抽滤时的操作为 。
为了证明在实验室制备Cl2的过程中会有水蒸气和HCl挥发出来,甲同学设计了如下图所示的实验装置,按要求回答问题。
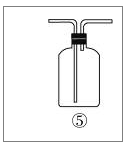
(1)请根据甲同学的意图,连接相应的装置,接口的顺序:b接___,___接___,___接a
(2)U形管中所盛试剂的化学式为_________________。
(3)装置③中CCl4的作用是________________。
(4)乙同学认为甲同学实验有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加装置⑤。你认为装置⑤应加在之间(填装置序号)。瓶中可以放入__________________。
(5)丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中AgNO3溶液
换成其它溶液。你认为可将溶液换成_____________,如果观察到____________
_________的现象,则证明制Cl2时有HCl挥发出来。
[实验化学]苯亚甲基苯乙酮俗称查尔酮,淡黄色梭状晶体,熔点58℃,沸点208℃(3.3kp),易溶于醚、氯仿和苯,微溶于醇。制备原理如下:

(1)制备过程中。需在搅拌下滴加苯甲酸,并控制滴加速度使反应温度维持在25~30℃,说明该反应是(填“放热”或“吸热”)反应。如温度过高时,则可采用措施。
(2)产品结晶前,可以加入几粒成品的查尔酮,其作用是。
(3)结晶完全后,需抽滤收集产物。’抽滤装置所包含的仪器除减压系统外还有、(填仪器名称)。
(4)获得的深色粗产品加入活性炭,用95%乙醇重结晶即得查尔酮晶体,可通过法来判断原料是否反应完全以及反应的转化率和选择性。
溴化钙在医药上用作中枢神经抑制药,实验室用“尿素法”制备溴化钙的主要流程如下:
溴化钙的部分溶解度数值如下:
| 温度 |
0℃ |
10℃ |
20℃ |
40℃ |
60℃ |
80℃ |
100℃ |
| 溶解度(g) |
125 |
132 |
143 |
213 |
278 |
295 |
312 |
(1)6Ca(OH)2+6Br250~70℃5CaBr2+6H2O+Ca(BrO3)2,每生成1 mol Ca(BrO3)2转移电子的物质的量为;50~70℃时,尿素[CO(NH2)2]将生成的Ca(BrO3)2还原为CaBr2,尿素被氧化为N2,该反应的化学方程式为。
(2)过滤所需的玻璃仪器有玻璃棒、,。
(3)加入氢溴酸调pH的作用是。
(4)操作I包括、、过滤、、干燥。
(5)“二氧化硫法”制备的氢溴酸粗品中常含有少量的溴和硫酸;请选用所提供的试剂,补充完整检验氢溴酸粗品中是否含有Br2相SO42-的实验方案。
限选下列试剂:氯水、淀粉KI溶液、CCl4、BaCl2溶液、稀盐酸、植物油。
硫铁矿烧渣的主要成分为Fe2O3、Fe3O4,以及少量SiO2、Al2O3等。由硫铁矿烧渣制备铁红(Fe2O3)的一种工艺流程如下:
已知:还原焙烧时,大部分Fe2O3、Fe3O4转化为FeO。
几种离子开始沉淀和完全沉淀时的pH如下表所示:
| 离子 |
开始沉淀时的pH |
完全沉淀时的pH |
| Fe2+ |
7.6 |
9.7 |
| Fe3+ |
2.7 |
3.7 |
| Al3+ |
3.8 |
4.7 |
(1)“酸浸、过滤”步骤中所得滤液中的金属阳离子有(填离子符号)。
(2)Fe粉除调pH外,另一个作用是;Fe粉调节溶液的pH为。
(3)“沉淀、过滤”步骤中生成FeCO3的离子方程式为;
所得滤液的主要溶质是(填化学式)。
(4)高温条件下,“氧化”步骤中发生反应的化学方程式为。
(14分)I.草酸晶体的组成可用H2C2O4·x H2O表示,为了测定x值,进行如下实验:
(1) 称取Wg草酸晶体,配成100.00mL水溶液
(2) 取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为amol·L—1的KMnO4溶液滴定至KMnO4不再褪色为止,所发生的反应为:
2 KMnO4 + 5 H2C2O4 + 3 H2SO4= K2SO4 + 10CO2↑ + 2MnSO4 + 8H2O
试回答:
①在滴定过程中若用去amol·L—1的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为mol·L—1,由此可计算x的值是。
②若滴定终点读数时俯视,则计算的x值可能会(偏大、偏小、无影响)。
Ⅱ.实验室用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:
提示:乙醇与浓硫酸在140℃时脱水生成乙醚,在170℃时脱水生成乙烯。
有关数据列表如下:
| 乙醇 |
1,2-二溴乙烷 |
乙醚 |
|
| 状态 |
无色液体 |
无色液体 |
无色液体 |
| 密度/g · cm-3 |
0.79 |
2.2 |
0.71 |
| 沸点/℃ |
78.5 |
132 |
34.6 |
| 熔点/℃ |
-130 |
9 |
-116 |
回答下列问题:
(1)装置D中发生主要反应的化学方程式为。
(2)装置B的作用,长玻璃管E的作用。
(3)在装置C中应加入,其目的是吸收反应中可能生成的酸性气体 (填正确选项前的字母)。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4) 反应过程中应用冷水冷却装置D,其主要目的是;但又不能过度冷却(如用冰水),其原因是;将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在层(填“上”、“下”)。
(5)若产物中有少量未反应的Br2,最好用洗涤除去 (填正确选项前的字母) 。
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇