某废金属屑中主要成分为Cu、Fe、Al,还含有少量的铜锈[Cu2(OH)2CO3]、少量的铁锈和少量的氧化铝,用上述废金属屑制取胆矾(CuSO4·5H2O)、无水AlCl3和铁红的过程如下图所示:
请回答:
(1)在废金属屑粉末中加入试剂A,生成气体1的反应的离子方程式是_________________。
(2)溶液2中含有的金属阳离子是__________;气体2的成分是______________。
(3)溶液2转化为固体3的反应的离子方程式是____________________________。
(4)利用固体2制取CuSO4溶液有多种方法。
①在固体2中加入浓H2SO4并加热,使固体2全部溶解得CuSO4溶液,反应的化学方程式是___________。
②在固体2中加入稀H2SO4后,通入O2并加热,使固体2全部溶解得CuSO4溶液,反应的离子方程式是_____________________________。
(5)溶液1转化为溶液4过程中,不在溶液1中直接加入试剂C,理由是__________________
(6)直接加热AlCl3·6H2O不能得到无水AlCl3。SOCl2为无色液体,极易与水反应生成HCl和一种具有漂白性的气体。AlCl3·6H2O与SOCl2混合加热制取无水AlCl3,反应的化学方程式是______________。
X、Y、Z、W四种化合物均由元素周期表前18号元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。
请回答:
(1)W的化学式是 。
(2)X与Y在溶液中反应的离子方程式是 。
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置III中生成白色沉淀,装置V中可收集到一种无色气体。
①装置I中反应的化学方程式是 。装置II中物质的化学式是 。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的位置V中气体,该化合物的化学式是 ,所需仪器装置是 (从上图选择必要装置,填写编号)。
A、B、C、D表示中学化学中的四种常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去)。
(1)若A为强碱溶液,其焰色反应显黄色,C常用作食品添加剂,请回答下列问题:
①反应Ⅱ的离子方程式是 。
②现有B和C的固体混合物 g,加热至质量不再改变时剩余固体为
g,加热至质量不再改变时剩余固体为 g,则B的质量分数为 。
g,则B的质量分数为 。
(2)若A、D均为单质,且A为黄绿色气体,D的一种红棕色氧化物常用作颜料,则:
①反应Ⅱ的离子方程式是 。
②取少许C溶液于试管中,滴入NaOH溶液并振荡,发生反应的化学方程式为: , 。
③检验B溶液中金属阳离子的方法是 。
下图中A~H均为中学化学中常见的物质,它们之间有如下转化关系。其中A、C均为金属单质,C与水反应生成D和最轻的气体,D、H的焰色反应均呈黄色,在通常状况下E(氢氧化物)跟NaOH或盐酸均可发生复分解反应。(反应过程中生成的水及其他产物已略去)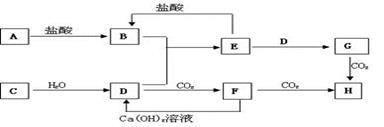
请回答以下问题:
(1)A是(填名称) ; H是(填化学式) 。
(2)请写出反应C→D的化学方程式,并用单线桥或双线桥法标明该反应中电子转移的方向和数目: 。
(3)Na2O2也可以生成D,写出其反应的化学方式: 。
(4)写出E转化为G的离子方程式: 。
(5)写出D转化为F的化学方程式: 。
(框图中A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色。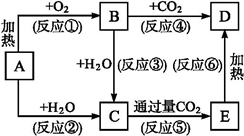
请填写下列空白:
(1)写出化学式:A ,B ,D 。
(2)以上反应中,属于氧化还原反应的有 (填编号)。
(3)写出E D的化学方程式: 。
D的化学方程式: 。
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。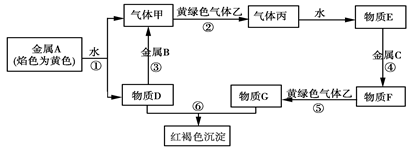
请根据以上信息回答下列问题:
(1)写出下列物质的化学式A________、B________、C________、乙________
(2)写出下列反应化学方程式:反应①__________________________________
反应③_________________________________
(3)写出下列反应离子方程式:反应④___________________
反应⑥_______________________