钛铁矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有少量MgO、CaO、SiO2等杂质。利用钛铁矿制备锂离子电池电极材料(钛酸锂Li4Ti5O12和磷酸亚铁锂LiFePO4)的工业流程如下图所示:

已知:FeTiO3与盐酸反应的离子方程式为:FeTiO3+4H++4Cl—= Fe2++ TiOCl42—+2H2O
(1)化合物FeTiO3中铁元素的化合价是___________。
(2)滤渣A的成分是___________。
(3)滤液B中TiOCl42-和水反应转化生成TiO2的离子方程式是 。
(4)反应②中固体TiO2转化成(NH4)2Ti5O15 溶液时,Ti元素的浸出率与反应温度的关系如图所示。反应温度过高时,Ti元素浸出率下降的原因 。

(5)反应③的化学方程式是 。
(6)由滤液D制备LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是___________。
(7)若采用钛酸锂(Li4Ti5O12)和磷酸亚铁锂(LiFePO4)作电极组成电池,其工作原理为:Li4Ti5O12 + 3LiFePO4 Li7Ti5O12 + 3FePO4 该电池充电时阳极反应式是: 。
Li7Ti5O12 + 3FePO4 该电池充电时阳极反应式是: 。
[化学—选修3:物质结构与性质]Fe2+、Fe3+与O22—、CN—、F—、有机分子等形成的化合物具有广泛的应用。
(1)N、O、F三种元素原子的第一电离能由大到小的顺序是。
(2)基态Fe3+核外M能层的电子排布式为。
(3)铁有δ、γ、α三种同素异形体(如下图),则γ晶胞原子堆积名称为_____________。假设各种晶型的铁单质都是由半径为r的铁原子堆积而成,则晶胞δ与晶胞α的密度比为_______________(列式并化简)。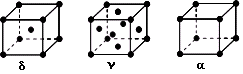
(4)乙酰基二茂铁是常用汽油抗震剂,其结构如图1所示。此物质中碳原子的杂化方式有。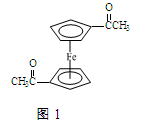
(5)配合物K3[Fe(CN)6]可用于电子传感器的制作。与配体互为等电子体的一种分子的电子式为。已知(CN)2是直线形分子,并具有对称性,则(CN)2中π键和σ键的个数比为。
(6)F—不仅可与Fe3+形成[FeF6]3—,还可以与Mg2+、K+形成一种立方晶系的离子晶体,此晶体应用于激光领域,结构如图2所示。该晶体的化学式为。在该晶体中与一个F—距离最近且相等的F—的个数为。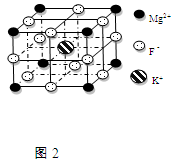
[化学—选修2:化学与技术]银、铜均属于重金属,从银铜合金废料中回收银并制备含铜化合物产品的工艺如图所示:
(1)熔炼时被氧化的元素是,酸浸时反应的离子方程式为。为提高酸浸时铜元素的浸出率及浸出速率,酸浸前应对渣料进行处理,其处理方法是。
(2)操作a是,固体B转化为CuAlO2的过程中,存在如下反应,请填写空白处:
CuO+Al2O3 +↑。
+↑。
(3)若残渣A中含有n mol Ag,将该残渣全部与足量的稀HNO3置于某容器中进行反应,写出反应的化学方程式。为彻底消除污染,可将反应中产生的气体与V L(标准状况)空气混合通入水中,则V至少为L(设空气中氧气的体积分数为0.2)。
(4)已知2Cu+ Cu+Cu2+,试分析CuAlO2分别与足量盐酸、稀硝酸混合后,产生现象的异同点。
Cu+Cu2+,试分析CuAlO2分别与足量盐酸、稀硝酸混合后,产生现象的异同点。
(5)假设粗银中的杂质只有少量的铜,利用电化学方法对其进行精炼,则粗银应与电源的极相连,当两个电极上质量变化值相差30.4g时,则两个电极上银质量的变化值相差g。
电解法促进橄榄石(主要成分是Mg2SiO4)固定CO2的部分工艺流程如下:
已知:Mg2SiO4(s) +4HCl(aq) 2MgCl2(aq) +SiO2 (s) + 2H2O(l)△H =-49.04 kJ·mol-1
2MgCl2(aq) +SiO2 (s) + 2H2O(l)△H =-49.04 kJ·mol-1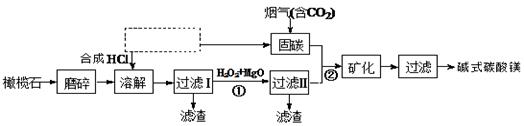
(1)橄榄石的组成是Mg9FeSi5O20,用氧化物的形式可表示为。
(2)上图虚框内需要补充一步工业生产的名称为。
(3)下列物质中也可用作“固碳”的是。(填字母)
a.CaCl2b.H2NCH2COONac.(NH4)2CO3
(4)由下图可知,90℃后曲线A溶解效率下降,分析其原因。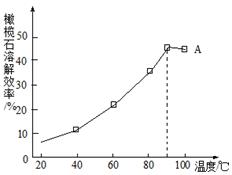
(5)过滤Ⅰ所得滤液中含有Fe2+,检验该离子方法为。
(6)过程①为除去滤液中的杂质,写出该除杂过程所涉及反应的离子方程式
、。
PM2.5污染跟工业燃煤密切相关,燃煤还同时排放大量的SO2和NOX。
(1)在一定条件下,SO2气体可被氧气氧化,每生成8 g SO3气体,放出9.83 kJ的热量,写出该反应的热化学方程式。若起始时向密闭容器内充入0.4molSO2和0.2mol O2,达平衡后放出的热量为Q,则Q39.32kJ(填“>”、“<”或“=”).
(2)一定条件下,在恒容密闭的容器中,当上述反应达到平衡时,下列说法正确的是__________(填序号)
a.2v逆(SO2)=v正(O2)
b.ΔH保持不变
c.混合气体密度保持不变
d.混合气体的平均相对分子质量保持不变
(3)500℃时,在催化剂存在条件下,分别将2 mol SO2和1 mol O2置于恒压容器I和恒容容器II中(两容器起始容积相同,),充分反应均达到平衡后,两容器中SO2的转化率关系是I_________II(填“>”、“<”或“=”)。若测得容器II中的压强减小了30%,则该容器中SO3体积分数为(结果保留3位有效数字)。
(4)将生成的SO3溶于水,再向溶液中通入NH3得到1L cmol/L(NH4)2SO4溶液的PH=5,计算该(NH4)2SO4溶液的水解平衡常数Kh=。
(5)NO2、O2和熔融NaNO3可制作原电池,其装置见下图。该电池中Na+向_____电极移动(填“Ⅰ”或“Ⅱ”),在电池使用过程中石墨I电极上生成氧化物Y,其电极反应为。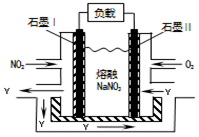
(1)已知:①CO(g)+2H2(g) CH3OH(g)△Hl= -91kJ·mol-l
CH3OH(g)△Hl= -91kJ·mol-l
②2CH3OH(g) CH3OCH3(g)+H2O(g)△H2= -24 kJ·mol-1
CH3OCH3(g)+H2O(g)△H2= -24 kJ·mol-1
③CO(g) +H2O(g)  CO2(g)+H2(g)△H3= -41 kJ·mol-l
CO2(g)+H2(g)△H3= -41 kJ·mol-l
且三个反应的平衡常数依次为K1、K2、K3
则反应 3CO(g) +3H2(g) CH3OCH3(g) +CO2(g)△H=
CH3OCH3(g) +CO2(g)△H=
化学平衡常数K=(用含K1、K2、K3的代数式表示)。
(2)写出反应②2CH3OH(g)  CH3OCH3(g)+H2O(g)平衡常数的表达式Kc=
CH3OCH3(g)+H2O(g)平衡常数的表达式Kc=
若在某温度下的平衡常数Kc = 400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 |
CH3OH |
CH3OCH3 |
H2O |
| c /mol·L-1 |
0.44 |
0.60 |
0.60 |
此时,v (正) _____ v (逆) (填“>”、“<”或“=”)。