某容器中发生一个化学反应,反应过程中存在H2O、ClO﹣、CN﹣、HCO3﹣、N2、Cl﹣六种离子。在反应过程中测得ClO﹣和N2的物质的量随时间变化的曲线如图所示.下列有关判断中不正确的是
| A.还原剂是含CN﹣的物质,氧化产物不只有N2 |
| B.氧化剂是ClO﹣,还原产物是HCO3﹣ |
| C.参与反应的氧化剂与还原剂的物质的量之比为5:2 |
| D.标准状况下若生成2.24LN2则转移电子1mol |
某温度时,在密闭容器中,X、Y、Z三种气体浓度的变化如图Ⅰ所示,若其它条件不变,当温度分别为T1和T2时,Y的体积分数与时间关系如图Ⅱ所示。则下列结论正确的是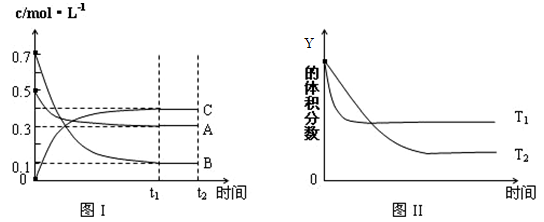
A.该反应的热化学方程式为:X(g)+3Y(g) 2Z(g);△H<0 2Z(g);△H<0 |
| B.若其它条件不变,升高温度,正、逆反应速率均增大,X的转化率增大 |
| C.达到平衡后,若其他条件不变,减小体积,平衡向逆反应方向移动 |
| D.达到平衡后,若其他条件不变,通入稀有气体,平衡向正反应方向移动 |
反应N2O4(g) 2NO2(g) △H=+57kJ/mol,在温度T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是
2NO2(g) △H=+57kJ/mol,在温度T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是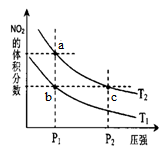
| A.a、c两点的反应速率:a>c |
| B.a、c两点气体的颜色:a浅,c深 |
| C.a、b两点气体的平均相对分子质量:a>b |
| D.b、c两点化学平衡常数:b<c |
对于可逆反应H2(g)+I2(g) 2HI(g),在一定温度下由H2(g)和I2(g)开始反应,下列说法正确的是
2HI(g),在一定温度下由H2(g)和I2(g)开始反应,下列说法正确的是
| A.H2(g)的消耗速率与HI(g)的生成速率之比为2:1 |
| B.正、逆反应速率的比值是恒定的 |
| C.反应进行的净速率是正、逆反应速率之差 |
| D.达到平衡时,正、逆反应速率相等 |
已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-Q1kJ/mol
2H2(g)+O2(g)=2H2O(g)△H=-Q2kJ/mol2H2(g)+O2(g)═2H2O(l)△H=-Q3kJ/mol
常温下,取体积比为4:1的甲烷和氢气的混合气体11.2L(已折合成标准状况),经完全燃烧后恢复至常温,则放出的热量为多少kJ
| A.0.4Q1+0.1Q3 | B.0.4Q1+0.05Q2 | C.0.4Q1+0.05Q3 | D.0.4Q1+0.1Q2 |
已知反应:①2C(s)+O2(g)="2CO(g)" △H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ/mol下列结论正确的是
| A.碳的燃烧热大于110.5 kJ/mol |
| B.①的反应热为221 kJ/mol |
| C.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ 热量 |
| D.稀硫酸与稀NaOH溶液反应的中和热为57.3 kJ/mol |