水的电离常数如图两条曲线所示,曲线中的点都符合c(OH一)×c(H+)=常数,下列说法错误的是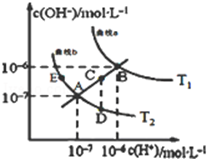
| A.图中温度T1>T2 |
| B.图中五点Kw间的关系:B>C>A=D=E |
| C.曲线a、b均代表纯水的电离情况 |
| D.若处在B点时,将pH=2的硫酸溶液与pH=12的KOH溶液等体积混合后,溶液显碱性 |
下列描述或化学用语书写错误的是
| A.向Fe(OH)3胶体中滴加稀硫酸,先生成红褐色沉淀,后沉淀逐渐溶解 |
| B.向铜粉中加入稀硫酸,铜粉不溶解,再加入硝酸钾固体,铜粉逐渐溶解 |
| C.氯碱工业和金属钠的冶炼都用到了NaCl,阳极上发生的电极反应都是:2Cl--2e-=Cl2↑ |
| D.向明矾(KAl(SO4)2·12H2O)溶液中滴入Ba(OH)2溶液,SO42-恰好完全沉淀时的离子方程式为: |
Ba2++3OH-+Al3++SO42-=BaSO4↓+Al(OH)3↓
下列说法错误的是
| A.同主族元素的简单阴离子还原性越强,水解程度越大 |
| B.Na和Cs属于IA族元素,Cs失电子的能力比Na强 |
| C.IA族与VIIA族元素间可形成共价化合物或离子化合物 |
| D.同周期元素(0族元素除外)从左到右,原子半径逐渐减小 |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.25℃时,pH=13的氨水中含有OH-的数目为0.1NA |
| B.标准状况下,2.24 LNO2与水反应生成NO3-的数目为0.1NA |
| C.1 mol Na被完全氧化生成Na2O2,转移电子的数目为NA |
| D.4.0 g H2与足量O2完全反应生成水,反应中断裂共价键的总数为2NA |
下列说法错误的是
| A.某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性 |
| B.等物质的量浓度的醋酸与醋酸钠溶液中水电离产生的c(OH-)前者小于后者 |
| C.沉淀溶解达到平衡时,溶液中溶质的离子浓度不一定相等,但保持不变 |
| D.水的离子积只与温度有关,向水中加入酸、碱或盐一定会影响水的电离平衡 |
化学与生产、生活、环境密切相关。下列说法错误的是
| A.航天飞机上的隔热陶瓷瓦属于复合材料 |
| B.硫酸钠溶液和氯化钡溶液均能使蛋白质变性 |
| C.“光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化物有关 |
| D.绿色化学的核心是利用化学原理从源头上减少或消除工业生产对环境的污染 |