实验室以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)为原料制取CaCl2·2H2O和CaO2的主要流程如下:
(1)加入试剂X,调节溶液pH为碱性环境,以除去溶液中Al3+和Fe3+,滤渣的主要成分是___________。试剂X可以选择下列的________(填编号)。
| A.CaO | B.CaCO3 | C.NH3·H2O | D.Ba(OH)2 |
(2)操作II中进行蒸发浓缩时,除三角架、酒精灯外,还需要的仪器有__________。
(3)由CaCl2制取CaO2的反应中,温度不宜太高的原因是_______________。
(4)用下列装置测定工业碳酸钙的质量分数
①检验装置B气密性良好的实验过程是__________________________。
②按A—B—C—D顺序连接,然后从A装置通入空气,目的是_______________;
③装置D的作用为______________________。
④实验时,准确称取10.00g工业碳酸钙3份,进行3次测定,测得BaCO3沉淀的平均质量为17.73g,则样品中CaCO3的质量分数为__________________。
某校化学小组学生进行如下实验。
(1)使用铜和稀硫酸制备硫酸铜晶体。
步骤如下:
步骤①观察到的现象是。步骤③的主要操作包括:。
(2)硫酸铜溶解度的测定。
用石墨电极(相同)电解饱和CuSO4溶液,阴极的电极反应式是。已知饱和CuSO4溶液的质量为60 g,通电10 min后,溶液恰好变为无色。称量发现两电极质量差为4 g,此温度下CuSO4的溶解度是。
(3)某同学查询资料得知:铜屑放入稀硫酸中不发生反应,若在稀硫酸中加入H2O2,铜屑可逐渐溶解。实验小组同学设计实验装置如图,验证该实验,该反应的化学方程式是。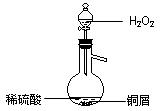
若将H2O2和稀硫酸加入烧瓶中的顺序颠倒,实验得到的结论是
。
利用如图所示的装置验证稀硝酸被铜还原的产物是NO而不是NO2:
(1)空气对实验影响很大。为了预先除去装置中的空气,在A装置中产生的气体是_________,检验装置中的空气已被除净的方法是___________________
_____________________________;E中应加入的试剂是_______________;
(2)关闭弹簧夹a和d,打开b,由分液漏斗向试管B中滴加稀硝酸,装置C中的气体呈__________色,装置D的作用是___________________________;关闭弹簧夹d的目的是__________________________________________;
(3)将A 装置换成鼓气球,鼓入少量空气,C中气体的颜色变为________色,此时弹簧夹b应打开,d应________(填“打开”或“关闭”);
(4)实验结束时,如何操作才能使装置中的有毒气体被E中的溶液充分吸收?
__________________________________________________________。
某校活动小组用下图所示装置及所给药品(图中夹持仪器已略去)探究工业制硫酸接触室中的反应,并测定此条件下二氧化硫的转化率。已知C中的浓硫酸含溶质m mol,假设气体进入C和D时分别被完全吸收,且忽略装置内空气中的CO2。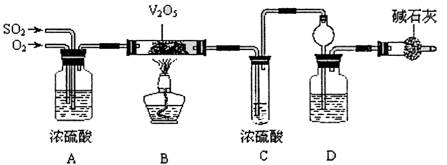
请回答下列问题:
(1)已知0.5 mol SO2被O2氧化成气态SO3,放出49.15kJ热量,反应的热化学方程式为。
(2)检查完装置的气密性且加入药品后,开始进行实验,此时首先应进行的操作是
。
(3)实验时A中氧气导冒出的气泡与二氧化硫导管冒出的气泡速率相近,其目的是
;装置C中浓硫酸的作用为;
装置D中盛放的溶液中足量的(选填字母)。
a.BaCl2溶液 b.NaOH溶液 c.NaHSO3饱和溶液
(4)停止通入SO2,熄灭酒精后,为使残留在装置中的SO2、SO3被充分吸收,操作方法是。
(5)实验结束后,稀释装置C中的溶液,并向其中加入足量的BaCl2溶液,得到的沉淀质量为wg。若装置D增加的质量为ag,则此条件下二氧化硫的转化率是
(用含字母的代数表示,结果可不化简)。
下图中,甲由C、H、O三种元素组成,元素的质量比为12:3:8,甲的沸点为78.5℃,其蒸气与H2的相对密度是23。将温度控制在400℃以下,按要求完成实验。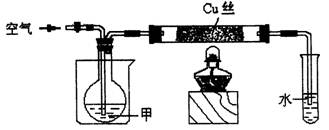
(1)在通入空气的条件下进行实验Ⅰ。
①甲的名称是 ,加入药品后的操作依次是 。
a.打开活塞 b.用鼓气气球不断鼓入空气 c.点燃酒精灯给铜丝加热
②实验结束,取试管中的溶液与新制的Cu(OH)2混合,加热至沸腾,实验现象为
。
③现用10%的NaOH溶液和2%的CuSO4溶液,制取本实验所用试剂Cu(OH)2,请简述实验操作。
。
(2)在停止通入空气的条件下进行实验Ⅱ。
①关闭活塞,为使甲持续进入反应管中,需要进行的操作是
。
②甲蒸气进入反应管后,在铜做催化剂有250~350℃条件下发生可逆的化学反应,
在试管中收集到了实验Ⅰ相同的产物,并有可燃性气体单质放出。该反应揭示了甲
催化氧化的本质。写出实验Ⅱ中反应的化学方程式,并结合该化学方程式简要说明实验Ⅰ中所通空气的作用。
某化学兴趣小组的同学,在学习了高中化学第三册中有关草酸的性质,查阅了大量资料,获得了草酸的一些信息,整理出下表:
| (1) 草酸晶体 |
分子式 |
H2C2O4·2H2O |
颜色 |
无色晶体 |
| 熔点 |
100.1℃ |
受热至100.1℃时失去结晶水,成为无水草酸。 |
||
| (2) 无水草酸 |
结构简式 |
HOOC—COOH |
溶解性 |
能溶于水或乙醇 |
| 特性 |
大约在157℃升华(175℃以上发生分解)。 |
|||
| 化学性质 |
H2C2O4 + Ba(OH)2 =BaC2O4↓+ 2H2O |
|||
| HOOC—COOH >175℃ CO2↑+CO↑+H2O↑ |
该组同学依据上表设计了一套如下图所示的实验装置,欲通过实验验证无水草酸受热分解的产物,并利用反应产生的CO气体来还原铁的某种氧化物(FexOy),以确定FexOy的组成。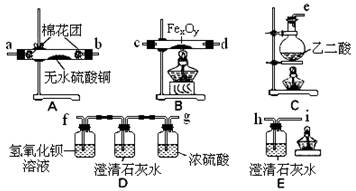
请回答下列问题:
(1)实验所需的仪器装置如上图所示,各装置的连接顺序为:
e接、接、接、接 h 。
(2)该组同学进行了下列实验操作:
①点燃B处的酒精灯;
②检查实验装置的气密性并装入药品;
③反应结束后,先熄灭B处的酒精灯,继续通入气体直到B中固体全部冷却后,再熄灭c处的酒精灯;
④点燃c处的酒精灯,开始反应,在装置E的i口处收集一试管气体,验纯;
⑤点燃尖嘴i处的酒精灯。
正确的实验操作顺序是:。
(3)收集气体验纯的目的是。
D装置中澄清石灰水的作用是。
E装置中澄清石灰水的作用是。
(4)反应完全后,该组同学进行数据处理。反应前,称得硬质玻璃管的质量为54.00 g,样品FexOy的质量为7.84 g;反应后,称得硬质玻璃管与剩余固体的总质量为59.60g(其质量经同样操作后也不再发生变化),则样品FexOy中,x:y=。
(5)本实验有没有不妥之处?如果有,请答出改进的方案;若无,此问可不必答。
。