下图是各种不同密度的硝酸与铁反应(相同温度)时主要还原产物的分布图。请认真读图分析,回答有关问题。
(1)下列叙述中正确的是(填序号) 。
| A.图中横坐标是硝酸的密度,硝酸的密度越大,其浓度越小。 |
| B.当还原剂和温度相同时,不同浓度的硝酸被还原的产物不是单一的,只是在某浓度时,以某种产物为主而已。 |
| C.硝酸的浓度越大,还原产物中N元素低化合价产物越少。 |
| D.当硝酸密度大于1.3 g·cm-3时,还原产物主要为NO、NO2 |
(2)当硝酸溶液的密度为1.36 g·cm-3时,Fe与过量硝酸反应的化学方程式是_________________。
(3)限用下列仪器、药品验证由铁和过量1.36 g·cm-3硝酸反应产生的气体中含有NO(不考虑N2O4)。设计一个合理而简单的实验方案(仪器可选择使用,N2的用量可自由控制,加热装置和固定装置省略)。
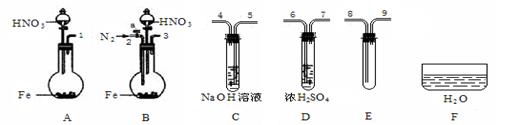
第1步:反应并收集生成的气体:
①实验中气体发生装置应选择 (填装置序号),理由是 。
②装置的连接顺序是(填各装置接口的序号):[ ]→[ ] [ ]→[8] [9]→[ ]。
③检查装置气密性后,开始反应。待E中充满红棕色气体,停止实验。
第2步:验证E中有NO。
④取下试管E,倒立在F中,轻轻摇动试管。
确认生成的气体中有NO的现象是 。
(4)某工厂生产硝酸的流程简要表示如下:
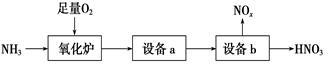
①氧化炉中反应的化学方程式为__________________________________。
②工业上通常用质量分数为15%的Na2CO3水溶液(密度1.16 g·mL-1)作为NOx吸收剂,它的物质的量浓度为_____________ mol·L-1(保留2位小数)。
下表是元素周期表的一部分,表中所列的字母分别代表某一种化学元素。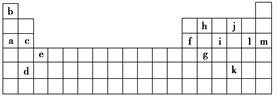
(1)上述第三周期元素中第一电离能(I1)最大的是________(用字母表示,下同),c和f的I1大小关系是________大于________。
(2)上述元素中,原子中未成对电子数最多的是________,写出该元素的电子排布式:________________。
(3)根据下表所提供的电离能数据,回答下列问题。
| 锂 |
X |
Y |
|
| I1 |
519 |
502 |
580 |
| I2 |
7296 |
4570 |
1820 |
| I3 |
11799 |
6920 |
2750 |
| I4 |
9550 |
11600 |
①表中X可能为以上13种元素中的________元素。用元素符号表示X和j形成的化合物的化学式________。
②Y是周期表中的________族的元素。
根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1)A元素次外层电子数是最外层电子数的1/4,外围电子的电子排布图是______。
(2)B是1~36号元素中原子核外电子排布未成对电子数最多的元素,B元素的名称是____,在元素周期表中的位置是____________________。
(3)C元素基态原子的电子排布图是下图中的_______(填序号),另一电子排布图不能作为基态原子的电子排布图是因为它不符合_______(填编号)。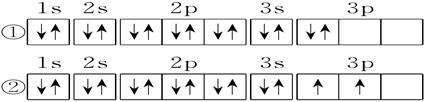
A.能量最低原理B.泡利原理 C.洪特规则
甲醇是一种可再生能源,具有广泛的开发和应用前景。请回答:
(1)工业上合成甲醇CO(g) + 2H2(g) CH3OH(g) ΔH,在不同温度下的化学平衡常数(K)如表所示。
CH3OH(g) ΔH,在不同温度下的化学平衡常数(K)如表所示。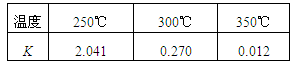
①根据表中数据可判断ΔH(填“>” 或 “=” 或 “<”)0。
②300℃时,向容积为1L的密闭容器中充入2 mol CO、3 mol H2和2 mol CH3OH,此时反应将。
A.向正方向移动B.向逆方向移动C.处于平衡状态
(2)已知在常温常压下:
①2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(l) ΔH= -a kJ·mol-1
②2CO (g)+ O2(g) = 2CO2(g)ΔH= -b kJ·mol-1
写出该条件下甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
。
(3)改变下列条件,能同时加快正反应的速率,增大CO的转化率的是
A.使用催化剂B.缩小容器体积
C.降低温度D.分离CH3OH的物质的量
(4)以甲醇、氧气为原料,KOH溶液作为电解质溶液构成燃料电池总反应为:2CH3OH +3O2+4OH- = 2CO32- + 6H2O,则负极的电极反应式为。
下图两个装置中用滴有酚酞的NaCl溶液做电解质溶液,进行化学能和电能相互转化的研究。请回答: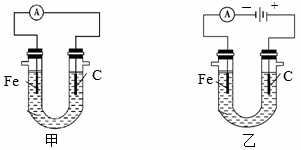
(1)写出两个铁电极上的电极反应式。
甲:
乙:
(2)甲装置中电极附近的溶液先变红,乙装置中电极附近的溶液先变红。
(3)检验乙中C电极反应产物的方法是。
(4)电解氯化钠稀溶液可制备“84消毒液”,通电时氯气被溶液完全吸收,若所得消毒液仅含一种溶质,写出相应的化学方程式:。所得消毒液中离子浓度的由大到小顺序。
(5)如果起始时乙中盛有足量一定浓度的CuSO4溶液,反应一段时间后,要使溶液恢复到以前的状态,可向溶液中加入一定量的(填化学式)。
下图是常见物质之间的转化关系。氧化物A是光导纤维的基本原料,单质Ⅰ、Ⅲ为非金属单质,单质Ⅱ为主族元素对应的金属单质。请回答:
(1)氧化物A的化学式:。单质Ⅱ与NaOH溶液反应的化学方程式。
(2)向盐甲的水溶液中通入过量的CO2,观察到的现象是 。
(3)单质Ⅰ的用途非常广泛,如用做(写一种即可)。
(4)盐乙的溶液呈现(填“酸性”或“碱性”或“中性”)。