配置一定物质的量浓度的NaOH溶液时,造成实验结果偏高的是( )
| A.定容时俯视液面 | B.容量瓶洗净后有少量水残留 |
| C.转移时没有洗涤烧杯和玻璃 | D.所用的氢氧化钠已吸水潮解 |
在温度一定、2L的恒容密闭容器中,发生3A(g)+B(g) 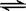 4C(g)+2D(s)的反应,若最初加入
4C(g)+2D(s)的反应,若最初加入
A和B都是2mol,10s时反应达到平衡,测得υ(A)=0.06mol/(L·S),则下列说法正确的是()
A.10s时,再加入一定量的D,平衡向右移动
B.10s时用D物质表示的速率为0.04mol/(L·S)
C.10s时,容器中B的浓度为1.6mol·L-1
D.达到平衡时A的转化率为60%,若要在相同条件下反应达到平衡时A的转化率仍为60%,起始
加入n(A)=n(B)即可
在一密闭容器中,反应 aA(g)  bB(g)达到平衡后,保持温度不变,将容器体积增大一倍,
bB(g)达到平衡后,保持温度不变,将容器体积增大一倍,
达到新的平衡时,B的浓度是原来的40%,则下列说法正确的是()
| A.平衡向正反应方向移动了 |
| B.物质A的转化率增加了 |
| C.物质B的质量分数减少了 |
| D.b>a |
强酸和强碱的稀溶液中和热可表示为:H+(aq)+OH-(aq)=H2O(l) ΔH= -57.3kJ/mol
以下4个化学方程式中: ①H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l)
②H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)
③NH3·H2O(aq)+HCl(aq)=NH4Cl(aq)+H2O(l)
④NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l) 其中反应热为-57.3kJ/mol的是()
| A.①② | B.③ | C.④ | D.均不符合 |
进入冬季,大雪也会引发巨大灾难。下列说法不正确的是( )
| A.雪是由水蒸气凝华而成的,该过程有能量放出 |
| B.雪融化为水后能量增加 |
| C.雪融化为水时要吸收能量,导致环境温度升高 |
| D.在雪上撒大量的盐(如NaCl、MgCl2等)可以融雪 |
当今国际能源研究的热点之一是寻找新能源,下列能源不属于新能源的是( )
| A.太阳能 | B.氢能 | C.风能 | D.天然气 |