1丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125 ℃,反应装置如图。下列对该实验的描述错误的是( )
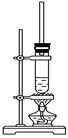
| A.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤 |
| B.加入过量乙酸可以提高1丁醇的转化率 |
| C.长玻璃管起冷凝回流作用 |
| D.不能用水浴加热 |
用NA表示阿伏加德罗常数,以下各说法中正确的是
| A.常温常压下,11.2 L氯气含有的分子数目大于0.5NA |
| B.常温常压下,2.24 L四氯化碳中所含氯原子数大于0.4 NA |
| C.0.1mol的铜与足量的浓硫酸反应生成SO2的体积约为22.4L |
| D.在同温同压下,相同体积的任何气体单质应含有相同的原子数 |
下列说法中不正确的是
| A.-NO2和NO2所含有的电子总数不相等 |
B.-OH和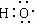 的化学性质相同 的化学性质相同 |
| C.HCOOCH3和CH3OCHO是同一物质 |
| D.若CH3+中所有的原子共平面,则其键角为120° |
下列各项表达式正确的是
A.乙炔的分子模型示意图: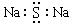 |
B.Na2S的电子式: |
C.NH4Cl的电子式: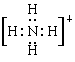 Cl- Cl- |
|
D.水的电离方程式:H2O+H2O H3O++OH— H3O++OH— |
将50g溶质质量分数为w1,物质的量浓度为c1的浓硫酸沿玻璃棒加入到Vml水中,稀释后得到溶质质量分数为w2,物质的量浓度为c2的稀溶液。下列说法中正确的是
| A.若c1 = 2c2,则w1<2w2,V<50 mL | B.若c1 = 2c2,则w1<2w2,V>50 mL |
| C.若w1 = 2w2,则c1<2c2,V="50" mL | D.若w1 = 2w2,则c1>2c2,V<50 mL |
阿伏加德罗常数(NA)、物质的量(n)和粒子数(N)之间有如下关系:NA=N/n,测定阿伏加德罗常数有多种方法,其中电解法是常用的方法。实验室有同样浓度的KCl、CuCl2、AgNO3、H2SO4等溶液,若实验过程中不考虑电极上的析出物与电解后的溶液之间的反应,则你认为选用哪一种溶液作为电解液,实验既简便、测定结果误差又小。
| A.KCl | B.CuCl2 | C.AgNO3 | D.H2SO4 |