聚乙烯醇Z是具有广泛用途的合成高分子材料,结构简式为 ,其工业合成路线如下:
,其工业合成路线如下:
已知:下列反应中R,R',R"代表烃基
i. 
ii. 
回答下列问题:
(1)乙炔的空间构型是____________;
(2)X的结构简式是_____________________;
(3)Y转化为Z的化学方程式是_____________________;
(4)在一定条件下,也可用乙烯、氧气和乙酸制取X,该反应的化学方程式是________________;
(5)已知:
在横线上填入物质、在方框内填上系数完成聚乙烯醇转化为维纶的化学方程式。
(14分) 卤化物和卤酸盐在工业生产中有着重要的作用。某小组为探究其中一些盐的性质,查阅资料并进行实验。查阅资料如下:
① BrO3- + 6I- + 6H+ = 3I2 + Br-+ 3H2O② 2BrO3- + I2 = 2IO3- + Br2
③ IO3- + 5I- + 6H+ = 3I2 + 3H2O ④ 2IO3- + 10Br-+ 12H+ = I2 + 5Br2 + 6H2O
实验如下:
| 步骤 |
现象 |
| ⅰ.向盛有30 mL 0.2 mol·L-1 KI溶液的锥形瓶中依次滴入几滴淀粉溶液和足量稀硫酸,再用滴定管逐滴加入KBrO3溶液 |
随着KBrO3溶液滴入,溶液由无色变为蓝色并逐渐加深,最终保持不变 |
| ⅱ.继续向上述溶液中滴入KBrO3溶液 |
溶液的蓝色逐渐褪去 |
请回答:
(1)步骤ⅰ开始时发生的反应如资料①所示,溶液中I-完全被氧化时转移mol电子,该反应中硫酸表现出的化学性质是。
(2)上述资料中的反应(填序号)可表示步骤ⅱ中的反应,通过该反应(填“能”或“不能”)说明碘的非金属性强于溴,原因是。
(3)根据资料中的反应①~④并结合所学知识,判断IO3-、BrO3-、I2、Br2的氧化性由强到弱的顺序是;KBrO3溶液与KBr溶液在酸性条件下反应的离子方程式是。
(4)若用y表示锥形瓶中含碘物质的物质的量,用x表示所滴入KBrO3的物质的量,在下图中画出上述整个实验过程中y随x的变化曲线(要求:在图中标出终点坐标)。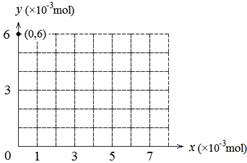
A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图所示(部分产物已略去)。
(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为。
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则 ①C的化学式为。
②反应B+A→C的离子方程式为。
(3)若A为强碱,D为气态氧化物。常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如上图的图b或图c所示(不考虑D的溶解和水的挥发)。
①若图b符合事实,则D为(填化学式),此时图b中x7(填“﹥”“﹤”“﹦”)
②若图c符合事实,则其pH变化的原因是(用离子方程式表示);
(4)若A为非金属单质,D是空气的主要成分之一。它们之间转化时能量变化如上图a,请写出A+D→C的热化学方程式:。
A、B、C、D、E代表单质或化合物,它们之间的相互转换关系如下图所示。A为地壳中含量仅次于氧的非金属元素的单质,其晶体结构与金刚石相似。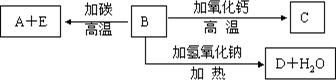
请填空:
(1)形成单质A的原子的结构示意图为,它的最高化合价为。
(2)B的化学式(分子式)为,B的晶体类型为。
B和碳反应生成A和E的化学方程式是。
(3)C的化学式(分子式)为,D的化学式(分子式)为。
(8分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO+4H++3e-→ NO+2H2O;KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:_______________________________。
(2)反应中硝酸体现了________、________的性质。
(3)反应中若产生0.2mol气体,则转移电子的物质的量是________mol。
(4)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是______________________。
(1)已知断开1 mol H2中的化学键需吸收436 kJ热量,断开1 mol Cl2中的化学键需要吸收243 kJ能量,而形成1 molHCl分子中的化学键要释放431 kJ能量,试求1 mol H2与1 mol Cl2反应的能量变化。△H= 。
(2)已知常温时,0.1mol/L某一元酸HA在水中有0.1%发生电离,则该溶液的PH=___①___,此酸的电离平衡常数K=___②___,由HA电离出来的H+的浓度约为水电离出来的H+的浓度的__③__倍。