甲醇(CH3OH)是一种重要的化工原料,广泛应用于化工生产,也可以直接用作燃料.已知:
CH3OH(l)+O2(g)===CO(g)+2H2O(g)ΔH1=-443.64 kJ/mol
2CO(g)+O2(g)===2CO2(g)ΔH2=-566.0 kJ/mol
(1)试写出CH3OH(l)在氧气中完全燃烧生成CO2和H2O(g)的热化学方程式_________________。
(2)科研人员新近开发出一种由强碱作电解质溶液的新型甲醇手机电池,可使手机连续使用一个月才充一次电,据此回答:甲醇在________极反应。
(3)利用电池可实现电能向化学能的转化。某同学设计了一种用电解法制取Fe(OH)2的实验装置(如图),通电后,溶液中产生大量的白色沉淀,且较长时间不变色.下列说法中不正确的是________(填序号)。
A.电源中的a一定为正极,b一定为负极
B.可以用NaCl溶液作为电解质溶液
C.A、B两端都必须用铁作电极
D.阴极发生的反应是2H++2e-===H2↑
铁是人类较早使用的金属之一,根据所学铁及其化合物的知识,回答下列问题:
(1)下列各物质中,不能和单质铝反应的物质是(填下列各项序号)。
①Fe②FeCl3③FeSO4
(2)向沸水中逐滴滴加1mol·L-1FeCl3溶液,至液体呈透明的红褐色,实验得到的分散系
属于(填“溶液”“浊液”或“胶体”),所得到的分散系中的分散质具有的性质有如下的(填写序号)。
①电泳②透过半透膜③聚沉④具有强还原性
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeCl3溶液与铜反应的化学方程式:;证明反应后的溶液中存在Fe3+的实验方法是。
现有下列六种物质,请根据要求填空(填写序号):
①氢氧化钠②氯化镁 ③二氧化碳 ④稀氨水 ⑤氢氧化铁胶体
(1)属于电解质的是
(2)属于混合物的是
(3)属于酸性氧化物的是
(10分)如图所示的实验装置中,E为一张用淀粉、碘化钾和酚酞混合溶液润湿的滤纸,C、D为夹在滤纸两端的铂夹;x、y分别为直流电源的两极。在A、B中充满KOH溶液后倒立于盛有KOH溶液的水槽中,再分别插入一多孔的惰性电极。切断电源开关S1,闭合开关S2,通直流电一段时间后,生成气体如图所示。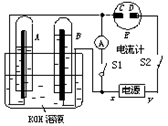
请回答下列问题:
(1)标出电源的正、负极:x为 。
(2)在滤纸的C端附近,观察到的现象是 。
(3)写出电极反应式:B电极 。
(4)若电解一段时间后,A、B中均有气体包围电极。此时切断开关S2闭合开关S1,则电流计的指针是否发生偏转 (填“偏转”或“不偏转”)。
(5)若电流计指针偏转,写出有关的电极反应(若指针“不偏转”,此题不必回答。);
。
若电流计指针不偏转,请说明理由(若指针“偏转”,此题不必回答) 。
为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题。
| 编号 |
操作 |
实验现象 |
| ① |
分别在试管A、B中加入5 mL 5% H2O2溶液,各滴入2滴1 mol/L FeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡。 |
试管A中不再产生气泡; 试管B中产生的气泡量增大。 |
| ② |
另取两支试管分别加入5 mL 5% H2O2溶液和5 mL 10% H2O2溶液 |
试管A、B中均未明显见到有 气泡产生。 |
(1)过氧化氢分解的化学方程式为__________________________________________。
(2)实验①的目的是______________________________________________________。实验中滴加FeCl3溶液的目的是_________________________________________。
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是_________________________________(用实验中所提供的几种试剂)。
(4)对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题: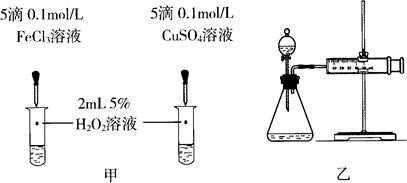
①定性分析:如图甲可通过观察_________________________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_________________________。
②定量分析:用图乙所示装置做对照实验,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是_________________________。
(9分)红磷P(s)和Cl2 (g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示
(图中的ΔH表示生成lmol产物的数据)。
根据上图回答下列问题:
(1) PCl5分解成PCl3 和Cl2的热化学方程式是______________;
上述分解反应是一个可逆反应。温度T1时,在密闭容器中加人0.80 mol PC15,反应达平衡时PC15还剩0.60 mol,其分解率α1等于________;若反应温度由Tl升高到T2,平衡时PC15的分解率α2为,α2_______α1(填“大于”、“小于”或“等于”) ;
(2)工业上制备PCl5通常分两步进行,先将P和Cl2反应生成中间产物PCl3,然后降温,再和Cl2反应生成PCl5原因是_______________________________________________
(3)P和Cl2分两步反应生成1molPCl5的ΔH3 =_____________________,P和Cl2一步反应生成1 mol PCl5的ΔH4___________ΔH3;(填“大于”、“小于”或“等于”)