在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g) 2SO3(g) ΔH<0,其它条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
2SO3(g) ΔH<0,其它条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
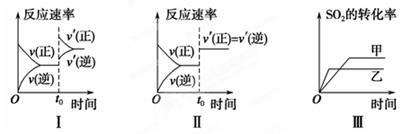
| A.图Ⅰ研究的是t0时刻增大O2的物质的量浓度对反应速率的影响 |
| B.图Ⅱ研究的是t0时刻通入氦气增大体系压强对反应速率的影响 |
| C.图Ⅲ研究的是催化剂对化学平衡的影响,且甲的催化效率比乙高 |
| D.图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高 |
下列化合物分子中,在核磁共振氢谱图中能给出三种信号峰的是
| A.CH3CH2CH3 | B.CH3COCH2CH3 | C.CH3CH2CH2OH | D.CH3OCH3 |
下列说法中正确的是
| A.凡能发生银镜反应的有机物一定是醛 |
| B.在氧气中燃烧时只生成CO2和H2O的物质一定是烃 |
| C.苯酚有弱酸性,俗称石炭酸,因此它是一种羧酸 |
| D.在酯化反应中,羧酸脱去羧基中的羟基,醇脱去羟基中的氢而生成水和酯 |
在烧焦的鱼、肉中含有致癌物质3,4一苯并芘,其结构简式如图所示,它是一种稠环芳香烃,其分子式是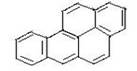
| A.C20H12 | B.C20H14 | C.C19H12 | D.C22H20 |
下图所示装置中观察到电流计指针偏转,M棒变粗,N棒变细,指针指向M,由此判断下表中所列M、N、P物质,其中可以成立的组合是

若只改变下列中的一个条件,能使N2(g)+3H2(g)  2NH3(g) △H<0平衡向逆反应方向移动的是
2NH3(g) △H<0平衡向逆反应方向移动的是
| A.升高温度 | B.增大压强 | C.增大NH3的浓度 | D.使用催化剂 |