工业生产中常用MnS作为沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s) CuS(s)+Mn2+(aq),下列说法错误的是( )
CuS(s)+Mn2+(aq),下列说法错误的是( )
| A.该反应达平衡时[Mn2+]=[Cu2+] |
| B.MnS的Ksp比CuS的Ksp大 |
| C.往平衡体系中加入少量CuSO4固体后,[Mn2+]变大 |
D.该反应的平衡常数K=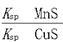 |
下列说法不正确的是( )
①质子数相同的粒子一定是同种元素
②同位素的性质几乎相同
③质子数相同,电子数也相同的两种粒子,不可能是一种分子和一种离子
④电子数相同的粒子不一定是同一种元素
⑤一种元素只能有一种质量数
⑥某种元素的相对原子质量取整数,就是其质量数
| A.②③⑤⑥ | B.①②④⑤ |
| C.①②⑤⑥ | D.③④⑤⑥ |
下列各组粒子:①H3O+,NH4+,Na+;②OH-,NH2-,F-;③O2-,Na+,Mg2+;④CH4,NH3,H2O。具有相同质子数和电子数的正确组合是( )
| A.①②③ | B.②③④ | C.①②④ | D.①③④ |
最近,我国某物理研究所取得重大科技成果,研制出由18O所形成的单质气体。18O是一种稳定的同位素,称为重氧。下列有关说法不正确的是( )
| A.1.8 g18O形成的气体的物质的量是0.05 mol |
| B.0.1 mol重氧水H218O所含的中子数约为6.02×l023个 |
| C.0.2 mol18O2气体的体积约为4.48 L |
| D.18O2气体的摩尔质量为36 g/mol |
若NA为阿伏加德罗常数,已知某元素的阴离子Rn-的原子核中,中子数为A-x+n,其中A为原子的质量数,则m g Rn-中电子总数为( )
A.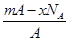 |
B.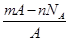 |
C.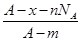 |
D.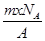 |
金属钛(Ti)被称为未来“钢铁”,也称为“太空金属”。对钛元素的同位素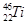 、
、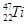 、
、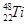 、
、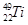 、
、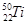 ,下列说法中不正确的是( )
,下列说法中不正确的是( )
| A.上述同位素中,Ti原子核中的中子数不可能为30 |
| B.题述中包括5种钛元素,且质子数都为22 |
| C.题述中包括5种钛原子,即钛元素的5种核素 |
| D.钛的相对原子质量不可能为46,也不可能为50 |