相同温度下,根据三种酸的电离常数,下列判断正确的是( )

| A.三种酸的强弱关系:HX>HY>HZ |
| B.反应HZ+Y﹣═HY+Z﹣能够发生 |
| C.相同温度下,0.1 mol·L﹣1的HX、HY、HZ溶液,HX与锌反应一定最快 |
| D.相同温度下,1 mol·L﹣1 HX溶液的电离常数大于0.1 mol·L﹣1 HX |
下列各组热化学方程式中,化学反应的△H前者大于后者的是
①C(s)+O2(g)===CO2(g);△H1
C(s)+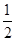 O2(g)===CO(g);△H2
O2(g)===CO(g);△H2
②S(s)+O2(g)===SO2(g);△H3
S(g)+O2(g)===SO2(g);△H4
③H2(g)+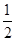 O2(g)===H2O(l);△H5
O2(g)===H2O(l);△H5
2H2(g)+O2(g)===2H2O(l);△H6
④CaCO3(s)===CaO(s)+CO2(g);△H7
CaO(s)+H2O(l)===Ca(OH)2(s);△H8
| A.① | B.④ | C.②③④ | D.①②③ |
下图是温度和压强对X+Y  2Z 反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
2Z 反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是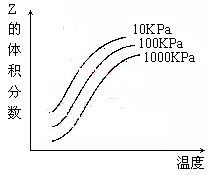
| A.上述可逆反应的正反应为放热反应 |
| B.X、Y、Z均为气态 |
| C.X和Y中只有一种是气态,Z为气态 |
| D.上述反应的逆反应的△H>0 |
常温下,向10mL pH=10的KOH溶液中加入pH=4的一元酸HA的溶液至pH刚好等于7(假设反应体积不变),则对反应后溶液的叙述错误的是
| A.c(A-)=c(K+) |
| B.c(K+)+c(H+)=c(OH-)+c(A-) |
| C.c(H+)=c(OH-)<c(K+)<c(A-) |
| D.V总≤20mL |
把0.05molNaOH固体分别加入到100mL下列液体中,溶液的导电能力变化最小的是
| A.自来水 | B.0.5mol/L盐酸 |
| C.0.5mol/L HAc溶液 | D.0.5mol/LKCl溶液 |
在一密闭容器中,反应aA(气)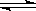 bB(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
bB(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
| A.平衡向正反应方向移动了 | B.物质A的转化率减少了 |
| C.物质B的质量分数减少了 | D.a>b |