反应CO+H2O(g) CO2+H2在1000K达到平衡时,分别改变下列条件,K值发生变化的是( )
CO2+H2在1000K达到平衡时,分别改变下列条件,K值发生变化的是( )
| A.将压强减小至原来的一半 | B.添加催化剂 |
| C.将反应温度升高至1200 K | D.增大水蒸气的浓度 |
下列事实不能用勒夏特列原理解释的是()
A.氯水中有平衡:Cl2+H2O HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅 HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅 |
B.对CO(g)+NO2(g) CO2(g)+NO(g),平衡体系增大压强可使颜色变深 CO2(g)+NO(g),平衡体系增大压强可使颜色变深 |
C.对2NO2(g)  N2O4(g), 升高温度平衡体系颜色变深 N2O4(g), 升高温度平衡体系颜色变深 |
| D.SO2催化氧化成SO3的反应,往往加入过量的空气 |
下列溶液中微粒的物质的量浓度关系正确的是()
| A.室温下,向0.01 mol·L-1 NH4HSO4溶液中滴加NaOH溶液至中性:C(Na+)+C(H+)+C(NH4+)=C(SO42-)+C(OH-) |
| B.0.01 mol·L-1NaHCO3溶液中:C(Na+)>C(OH-)>C(HCO3-)>C(H+) |
| C.Na2CO3溶液中:C(OH-)= C(HCO3-)+2C(H2CO3)+ C(H+) |
| D.25℃时,浓度均为0.1 mol·L-1的CH3COOH、CH3COONa溶液等体积混合,溶液呈酸性:C(Na+)>C(CH3COOH) >C(CH3COO-)>C(H+)>C(OH-) |
下列说法合理的是()
A.增加反应物的用量,化学反应速率一定加快
B.在等浓度NaCl和Na2CrO4稀溶液中滴加AgNO3溶液,先析出AgCl,则KSP(AgCl)<KSP(Ag2CrO4)
C.难溶物A.B,KSP(A)>KSP(B),则溶解度S(A)>S(B)
D.将碳酸钠溶液和碳酸氢钠溶液分别蒸干并灼烧,所得固体的成分均为碳酸钠
在一定条件下,Na2CO3溶液中存在水解平衡:CO32-+H2O HCO3-+OH-,下列说法正确的是()
HCO3-+OH-,下列说法正确的是()
| A.稀释溶液,水解平衡常数增大 | B.通入CO2,平衡朝正反应方向移动 |
C.升高温度,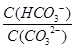 减小 减小 |
D.加入NaOH固体,溶液pH减小 |
pH="2" 的两弱酸HA.HB加水稀释后,溶液 pH随加水量的变化曲线如图所示。则下列叙述正确的是:()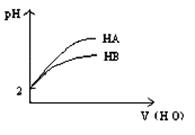
A.电离平衡常数HA > HB
B.等体积等pH的HA 和HB与等浓度的NaOH反应,HA消耗的NaOH多
C.等体积等pH的HA和HB 与等质量的Zn反应,HA反应速率大
D.若有等浓度的NaA.NaB,则碱性NaA>NaB