在0.1mol·L-1 CH3COOH溶液中存在如下电离平衡:CH3COOH  CH3COO-+H+
CH3COO-+H+
对于该平衡,下列叙述正确的是
| A.温度升高,平衡向逆反应方向移动 |
| B.加入少量NaOH固体,平衡向正反应方向移动 |
| C.加入少量0.1mol·L-1 HCl溶液,溶液中c(H+)减小 |
| D.加入少量醋酸钠固体,CH3COOH溶液的电离度增大 |
按下图装置,持续通入X气体,可以看到a处有红色物质生成,b处变蓝,c处得到液体,则X气体可能是()
| A.H2 | B.CO和H2 | C.NH3 | D.CH3CH2OH(气) |
某有机物的结构简式为: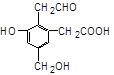
等物质的量的该物质分别与足量的Na、NaOH、新制Cu(OH)2反应,则需三种物质的物质的量之比为
| A.6∶4∶5 | B.1∶1∶1 | C.3∶2∶2 | D.3∶2∶3 |
以NA表示阿伏加德罗常数,下列说法正确的是()
| A.如果5.6L N2含有n个氮分子,则阿伏加德罗常数一定约为4n |
| B.15.6g Na2O2与过量CO2反应时,转移的电子数为0.2NA |
| C.1L 1mol/L 的FeCl3溶液中含有铁离子的数目为NA |
| D.1mol的甲烷中含有的C—H共价键的数目为6NA |
下列离子方程式中正确的是()
| A.过量的NaHSO4与Ba(OH)2溶液反应:Ba2++ 2 OH-+ 2 H+ + SO42-= BaSO4↓+2 H2O |
| B.NH4HCO3溶液与过量NaOH溶液反应:NH4+ + OH-= NH3↑+ H2O |
| C.硫化钠溶于水中:S2- + 2 H2O = H2S↑ + 2 OH- |
| D.FeBr2溶液中通入过量Cl2:2 Fe2+ + 2 Br- + 2 Cl2 =" 2" Fe3+ + Br2 + 4 Cl- |
下列离子在溶液中能大量共存的是()
| A.Fe3+、NH4+、Br-、SCN- | B.Na+、HCO3-、CO32-、K+ |
| C.Ca2+、CH3COO-、Cl-、K+ | D.S2-、Na+、ClO-、K+ |