25时,如果取0.1 mol·L-1HA溶液与0.1 mol·L-1NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因 (用离子方程式表示);
(2)混合溶液中由水电离出的c(H+)__0.1 mol·L-1 NaOH溶液中由水电离出的c(H+);(填>、<、=)
(3)求出混合液中下列算式的精确计算结果(填具体数字):c (Na+)-c (A-)= mol·L-1;
(4)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH 7 (填>、<、=);
(5)将相同温度下相同浓度的四种盐溶液:
| A.NH4HCO3 | B.NH4A | C.(NH4)2SO4 | D.NH4Cl |
按pH由大到小的顺序排列 (填序号)
(1)一个典型的病毒粒子的直径是5×10-6cm,如果把阿伏加德罗常数个这种病毒排成一行,其长度为_________ km。
(2)4.19 g某二价金属氯化物(ACl2)中含有0.4 mol Cl-,则ACl2的摩尔质量是_________;A的相对原子质量是_________;ACl2的化学式是__________________。
19g某二价金属氯化物(ACl2)中含有0.4 mol Cl ,则ACl2的摩尔质量是;A的相对原子质量是;ACl2的化学式是。
,则ACl2的摩尔质量是;A的相对原子质量是;ACl2的化学式是。
下表是某种常见金属的部分性质:
| 颜色状态 |
硬度 |
密度 |
熔点 |
导电性 |
导热性 |
延展性 |
| 银白色固体 |
较软 |
2.70 g·cm-3 |
660.4 ℃ |
良好 |
良好 |
良好 |
将该金属投入冷水中无变化,投入稀盐酸中,可产生大量的无色气体。根据上述信息完成下列问题:
(1)试推断该金属可能的一种用途________,该金属的活动性比铜_____________(填“强”或“弱”)。(2)请自选试剂,设计实验探究该金属与铁的活动性强弱,并完成下表:
| 猜想 |
验证方法 |
实验现象 |
| 该金属比铁活泼 |
||
| 该金属活泼性比铁弱 |
粉末状样品A是由等物质的量的MgO和Al2O3与常见金属氧化物B组成的混合物。A有如下图所示的转化关系。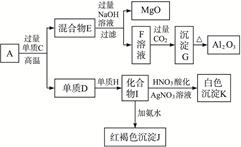
请完成下列问题:
(1)单质C和H的化学式分别是__________、__________。
(2)写出由I生成J的离子方程式:_____________。
(3)写出由F生成G的离子方程式:________。
(4)若10.7 g样品A中MgO、Al2O3和B的物质的量均为0.05 mol,则B的化学式为_________。
(5)若B中金属原子与氧原子的粒子数之比为2∶3,取7.10 g样品A,恰好与含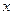 mol HCl的盐酸完全反应,则
mol HCl的盐酸完全反应,则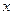 的取值范围是___________(保留小数点后两位)。
的取值范围是___________(保留小数点后两位)。
据说古代有一队运输纯碱的车队,夜晚在沙滩上用纯碱块和石块打起炉灶烧火做饭,第二天清晨日出时,在炉灶处发现有些明晃晃的东西
(1)你认为明晃晃的东西是______________。
(2)写出整个过程中的化学方程式:____________。