在下图转化关系中,已知B、D都是淡黄色固体,请回答下列问题。
⑴写出下列物质的化学式:B ,G 。
⑵写出下列反应的化学方程式:
A→B: ;E→F: ;B→C: 。
⑶将过量气体E通入到下列各组溶液后,离子仍能大量共存的是 。
A.Ba2+、Ca2+、Cl- B.OH-、CO32-、Na+
C.Ca2+、ClO-、Cl- D.H+、Fe3+、NO3-
某药品标签上贴有 OTC,它表示_____________________,若是R标记则表示________ __,我们平时能自己到药店买到的药如阿司匹林属于哪类药__________________。
OTC,它表示_____________________,若是R标记则表示________ __,我们平时能自己到药店买到的药如阿司匹林属于哪类药__________________。
(14分)已知A、B、C、D、E是短周期的5种元素,它们的原子序数依次增大。A元素原子形成的离子核外电子数为零;C、D、E三种元素的最高价氧化物对应水化物之间可以两两反应;A与C同主族;B与E同主族;E的单质为黄色晶体,易溶于二硫化碳。
(1)请写出B、D元素的名称:B,D。
(2)画出C元素的离子结构示意图。
(3)写出D的单质与C的最高价氧化物对应水化物之间反应的离子方程式
(4)A、B、C三种元素形成的化合物为,所含的化 学键类型为。
学键类型为。
(5)B、C、D三种元素的离子半径由大到小的排列顺序为(用离子符号表示)。
Ⅰ用元素符号或化学式回答原子序数11~18的元素的有关问题:
(1)除稀有气体外,原子半径最大的元素是________________;
(2)最高价氧化物对应水化物呈两性的元素是________________;
(3)最高正 价氧化物对应水化物酸性最强的酸是________________;
价氧化物对应水化物酸性最强的酸是________________;
(4)能形成气态氢化物且氢化物最稳定的元素是____ ____________。
____________。
Ⅱ在MgCl2和AlCl3的混和溶液中,逐滴加入NaOH溶液直至过量,经测定,加入NaOH的物质的量和所得沉淀的物质的量的关系如下图所示,则溶液中n(Mg2+):n(Al3+)= ,AB段发生的离子反应为。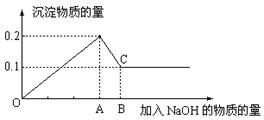
重铬酸钾是工业生产和实验室的重要氧化剂,工业上常用铬铁矿(主要成份为FeO·Cr2O3)为原料生产,实验室模拟工业法用铬铁矿制K2Cr2O7的主要工艺如下,涉及的主要反应是:6FeO·Cr2O3+24NaOH+7KClO3 12Na2CrO4+3Fe2O3 +7KCl+12H2O,
12Na2CrO4+3Fe2O3 +7KCl+12H2O,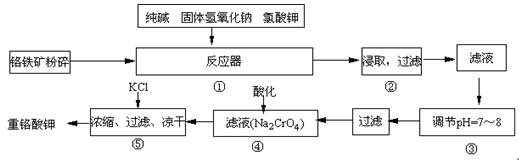
试回答下列问题:
(1)在反应器①中,有Na2CrO4生成,同时Fe2O3转变为NaFeO2,杂质SiO2、Al2O3与纯碱反应转变为可溶性盐,写出氧化铝与碳酸钠反应的化学方程式:
。
(2)操作③的目的是什么,用简要的文字说明:
。
(3)操作④中,酸化时,CrO42-转化为Cr2O72-,写出平衡转化的离子方程式:
。
(4)称取重铬酸钾试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL 2mol/LH2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol/LNa2S2O3标准溶液滴定。
(I2+2S2O32-=2I-+S4O62-)
①判断达到滴定终点的依据是:;
②若实验中共用去Na2S2O3标准溶液40.00mL,则所得产品中重铬酸钾的纯度(设整个过程中其它杂质不参与反应)%(保留小数点后两位)。
(15分)铝、铁、铜是应用最普遍的金属。
(1)铜是印刷电路工业的重要材料。用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜,是工业上采用的方法之一。已知
Cu(s) + 2H+(aq) ="=" Cu2+(aq) + H2(g)△H= +64.39kJ/mol
2H2O2(l) ="=" 2H2O(l) + O2 (g)△H= ﹣196.46kJ/mol
H2(g) +1/2 O2 (g)="=" H2O(l)△H= ﹣285.84kJ/mol
在H2SO4溶液中Cu和H2O2反应生成Cu2+和H2O的热化学方程式为
(2)镁铝合金生活中应用广泛。取样品a克,溶于200ml 5mol/L的HCl溶液,收集到标况下氢气3.36L,a的取值范围,向反应后溶液中加入4mol/L NaOH溶液ml,沉淀质量达到最 大
大 值。
值。
(3)标准状况下,铁铜合金ag加入足量稀硝酸中,收集了一定量气体NO,在混合了67 .2mlO2后,可完全被H2O吸收,无气体剩余。则生成的NO为ml;向反应后溶液加足量的NaOH溶液,得到沉淀的质量g。(用含a的代数式表示)
.2mlO2后,可完全被H2O吸收,无气体剩余。则生成的NO为ml;向反应后溶液加足量的NaOH溶液,得到沉淀的质量g。(用含a的代数式表示)