(1)人们常用催化剂来选择反应进行的方向,左图所示为一定条件下1molCH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去].
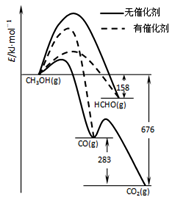
①写出1moL HCHO与O2发生反应时生成CO和H2O(g)的热化学方程式_______________;
②CH3OH与O2在有催化剂作用下反应,产物中HCHO比率大大提高的原因是_______________;
(2)①一定温度下,将N2H4与NO2以体积比为1:1置于10L定容容器中发生反应2N2H4(g)+2NO2(g) 3N2(g)+4H2O(l)△H<0,下列能说明反应达到平衡状态的是_______;
3N2(g)+4H2O(l)△H<0,下列能说明反应达到平衡状态的是_______;
A.混合气体密度保持不变 B.2v正(NO2)=3v逆(N2)
C.N2H4与NO2体积比保持不变 D.体系压强保持不变
②在某温度下,10L密闭容器中发生上述反应,容器内部分物质的物质的量变化如下表:
| 物质的量/mol 时间 |
n (N2H4) |
n (NO2) |
n (N2) |
| 起始 |
2.0 |
3.0 |
0 |
| 第2min |
1.5 |
a |
0.75 |
| 第4min |
1.2 |
b |
1.2 |
| 第6min |
1.0 |
c |
1.5 |
| 第7min |
1.0 |
c |
1.5 |
ⅰ前2min内NO2的平均反应速率为_____________(保留2位有效数字,下同)该温度下反应的平衡常数K=___________________。
ⅱ关于上述反应,下列叙述不正确的是_____________。
A.达到平衡时,移走部分N2,平衡将向右移动,正反应速率加快
B.缩小容器的体积,平衡向右移动,c(N2H4)将变大
C.在相同条件下,若使用甲催化剂能使正反应速率加快105倍,使用乙催化剂能使逆反应速率加快108倍,应选用乙催化剂
D.若保持平衡时的温度和压强不变,再向容器中充入He,则此时v(逆) >v(正)
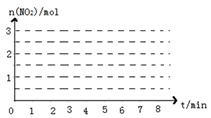
ⅲ.请画出该反应中n(NO2)随时间变化曲线,并画出在第7min分别升温、加压、加催化剂的情况下n(NO2)随时间变化示意图如图(在图上注明变化的条件)。
(1)BN是一种新型的无机材料,由于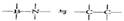 属等电子体物质,其结构和性质具有极大的相似性,则可推知,在BN的两种晶型中,一种是类似_________的空间网状结构晶体,可用作耐磨材料;另一种是类似于_________的层状结构的混合型晶体,可作用润滑材料,在其结构的每一层上最小的封闭环中有 _________个B原子,B—N键键角为_________。
属等电子体物质,其结构和性质具有极大的相似性,则可推知,在BN的两种晶型中,一种是类似_________的空间网状结构晶体,可用作耐磨材料;另一种是类似于_________的层状结构的混合型晶体,可作用润滑材料,在其结构的每一层上最小的封闭环中有 _________个B原子,B—N键键角为_________。
(2)单质硼有无定形体和晶体两种,参考下表数据。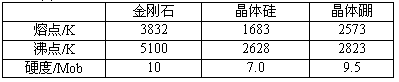
①晶体硼的晶体类型属于晶体,理由是_________。
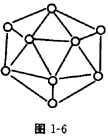
②已知晶体硼的基本结构单元是由硼原子组成的正二十面体(如图1—6所示),其中有20个等边三角形的面和一定数目的顶点,每个顶点上各有1个硼原子。通过观察图形及推算,此基本结构单元由_________个硼原子构成。其中B—B键的键角为_________。
二氧化硅晶体中,每个硅原子周围有_________个氧原子,每个氧原子周围有_________个硅原子,硅氧原子个数比为_________。若去掉二氧化硅晶体中的氧原子,且把硅原子看做碳原子,则所得空间网状结构与金刚石空间网状结构相同,试推测每个硅原子与它周围的4个氧原子所形成的空间结构为_________型;并推算二氧化硅晶体中最小的硅氧原子环上共有_________个原子。
(1)画出这两种固体分子的几何构型图:_________。
(2)黄绿色固体溶解度大的原因是:_________。
(1)下图为CO2分子晶体结构的一部分。观察图形,试说明每个CO2分子周围有个与之紧邻等距的CO2分子。
(2)试判断:①CO2、②CS2、③SiO2晶体的沸点由高到低排列的顺序是>>(填写相应物质的编号)。
(海水电池)1991年我国首创以铝-空气-海水电池作为能源的新型海水标志灯,以海水为电解质,靠空气中的氧气使铝不断氧化而产生电流,只要把灯放入海水中数分钟,就会发出耀眼的白光,则电源负极材料为:,正极材料为:。正、负极反应分别为:、。