大气污染越来越成为人们关注的问题,烟气中的NOx必须脱除(即脱硝)后才能排放。
(1)已知:CH4(g)+2O2(g)===CO2(g)+2H2O(1) ΔH=-890.3 kJ·mol-1
N2(g)+O2(g)==="2NO(g)" ΔH=+180 kJ·mol-1
CH4可用于脱硝,其热化学方程式为:CH4(g)+4NO(g)=CO2(g)+2N2(g)+2H2O(1),ΔH=________。
(2)C2H4也可用于烟气脱硝。为研究温度、催化剂中Cu2+负载量对NO去除率的影响,控制其它条件一定,实验结果如图1所示。为达到最高的NO去除率,应选择的反应温度和Cu2+负载量分别是___________________________。


(3)臭氧也可用于烟气脱硝。
①O3氧化NO 结合水洗可产生HNO3和O2,该反应的化学方程式为______________。
②一种臭氧发生装置原理如图2所示。阳极(惰性电极)的电极反应式为___________。
(4)如图3是一种用NH3脱除烟气中NO的原理。

①该脱硝原理中,NO最终转化为________(填化学式)和H2O。
②当消耗2molNH3和0.5molO2时,除去的NO在标准状况下的体积为_____________。
(5)NO直接催化分解(生成N2与O2)也是一种脱硝途径。在不同条件下,NO的分解产物不同。在高压下,NO在40 ℃下分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图4所示。写出Y和Z的化学式: _____________________________。
下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。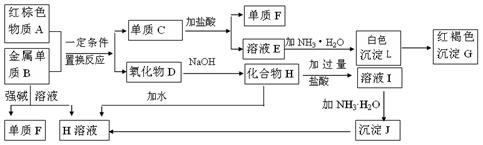
(1)单质B的化学式是,写出物质A的一种用途。
(2)写出单质B与强碱溶液反应的离子方程式,
写出由沉淀J生成 H溶液的离子方程式。
(3)写出白色沉淀L变为红褐色沉淀G的化学反应方程式
。
实验室要配制100 mL 2 mol/L NaCl溶液,请回答下列问题
(1)制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、胶头滴管、量筒和。
(2)用托盘天平称取氯化钠固体,其质量为g。
(3)若定容时俯视容量瓶刻度线,会造成所配溶液的物质的量浓度_________(偏大、偏小或无影响)。
某待测液中可能含有Ag+、Fe3+、K+、Ba2+、NH4+等阳离子,阴离子为NO3-,进行如下实验:
(1)加入过量的稀盐酸,有白色沉淀生成。
(2)过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成。
(3)过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现。
(4)另取少量步骤(3)中的滤液,加入NaOH溶液至使溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
根据实验现象回答:
待测液中一定含有离子,一定不含有离子,还有一种离子不能确定是否存在,要检验这种离子的实验方法是。
(共14分)
I . 为除去下列物质中所混有的少量杂质,写出选择的试剂并写出有关离子方程式。
(1)铁粉中混有少量SiO2,可选用试剂,
离子方程式;
(2)FeCl3溶液中混有少量FeCl2,可选用试剂,
离子方程式。
II . 将下列H2SO4性质的序号,填入各小题后面对应的横线上。
| A.脱水性 | B.强酸性 | C.难挥发性 | D.氧化性 E.吸水性 |
(1)用浓H2SO4可以干燥SO2气体
(2)在烧杯中放入蔗糖,滴入浓H2SO4,变黑色
(3)在冷的浓H2SO4中放入铝片没有明显现象
III . KClO3和浓盐酸在常温下反应生成氯气:KClO3+6HCl(浓)=" KCl+" 3Cl2↑+ 3H2O
(1)氧化剂是,还原产物是。
(2)若有12.25g KClO3发生反应,则转移的电子的物质的量为mol
(3)下列物质能使干燥的蓝色石蕊试纸先变红再褪色的是(填序号)
①氯气 ②液氯 ③新制氯水 ④敞口放置的久置氯水 ⑤盐酸 ⑥加了醋酸的漂白粉溶液
某实验活动小组在实验室进行中和 反应反应热的测定。请回答下列问题:
反应反应热的测定。请回答下列问题:
(1)测定中和反应反应热的实验装置如图所示。在两个烧杯之间填弃碎泡沫塑料的目的是。
(2)在进行中和反应反应热的测定中,量取50 mL 0.50mol/L的盐酸,倒入小烧杯中,测量盐酸的温度,然后需加入下列试剂(填序号)
①50mL 0.50mol/L NaOH溶液
②50mL 0.55mol/L NaOH溶液
③1.0g NaOH固体
(3)下述情况会使中和反应反应热的测定结果偏小的是(填序号)
a.用量筒量取50mL 0.50mol/L的盐酸时仰视读数
b.分多次把(2)中所选试剂倒入盛有盐酸的小烧杯中
c.用醋酸代替盐酸