Ⅰ.二氧化锰是化学工业中常用的氧化剂和催化剂,其主要制备方法是碳酸锰热分解,反应原理为2MnCO3(s)+O2(g) 2MnO2(s)+2CO2(g)。经研究发现该反应过程为:① MnCO3(s)
2MnO2(s)+2CO2(g)。经研究发现该反应过程为:① MnCO3(s)  MnO(s) + CO2(g) ②2MnO(s) + O2(g)
MnO(s) + CO2(g) ②2MnO(s) + O2(g)  2MnO2(s)
2MnO2(s)
(1)反应①达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是 。(填字母序号)
| A.平衡常数减小 | B.MnCO3质量不变 | C.CO2压强不变 | D.MnCO3物质的量增加 |
(2)反应②在低温下能自发进行,则其△H 0(填“>”、“<”、“=”)。
(3)某温度下,该平衡体系的总压强为P,CO2、O2的物质的量分别为n1和n2,用平衡分压代替平衡浓度,则碳酸锰热分解总反应的化学平衡常数Kp= (提示:用含P、n1、n2 的字母表达, 分压 = 总压×物质的量分数)
Ⅱ. 软锰矿(主要成分MnO2,杂质金属元素Fe、Al、Mg等)的悬浊液与烟气中SO2反应可制备MnSO4·H2O。

(4)已知:Ksp[Al(OH)3] =1×10-33,Ksp[Fe(OH)3] =3×10‾39,pH =7.1时Mn(OH)2开始沉淀,pH =9.4时Mg(OH)2开始沉淀。室温下,除去MnSO4溶液中的Fe3+、Al3+( 欲使其浓度小于1×10-6 mol·L-1),需调节溶液pH范围为_______________________。
(5)由右图可以看出,从MnSO4和MgSO4混合溶液中结晶MnSO4·H2O晶体,需控制结晶温度范围为 Ⅰ. 。Ⅲ. 二氧化锰也是电化学的重要材料。
(6)碱性锌锰电池的总反应是:Zn + 2MnO2 + 2H2O ="=" 2MnOOH + Zn(OH)2,该电池正极的电极反应为 。
Ⅰ.下列各项分别与哪个影响化学反应速率因素的关系最为密切?
⑴夏天的食品易变霉,在冬天不易发生该现象_________
⑵同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢
⑶MnO2加入双氧水中放出气泡更快______________。
Ⅱ.在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图所示:
⑴比较t2时刻,正逆反应速率大小V正____ V逆。(填“>”、“=”、“<”)
⑵若t2 =2min,计算反应开始至t2时刻,M的平均化学反应速率为:________
⑶t3时刻化学反应达到平衡时反应物的转化率为_________
⑷如果升高温度则V逆____(填增大、减小或不变)
Ⅰ.下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的某性质)
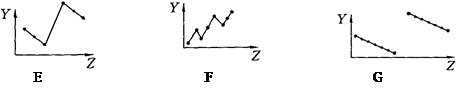
把与下面元素有关性质相符的曲线标号填入相应括号中:
⑴ⅡA族元素的最外层电子数 ( )⑵第三周期元素的最高化合价()
⑶第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径()
⑷第二、三周期元素随原子序数递增原子半径的变化(不包括惰性气体) ()
⑸碱金属的阳离子氧化能力(不包括钫)()
Ⅱ.下图是元素周期表的一部分
 |
|||||||||||||||||
⑴请在表中画出金属与非金属的交界线⑵请在表中标出第VIII的位置
⑶在表中标出 的位置
的位置
下面是用98%的浓H2SO4(ρ=1.84g/cm3)配制成0.5mol/L的稀H2SO4500ml的操作,请按要求填空:
(1)所需浓H2SO4的体积为
(2)如果实验室有15mL、20mL、50mL量筒,应选用mL量筒最好。量取时发现量筒不干净,用水洗净后直接量取,所配溶液浓度将(偏高、偏低、无影响)。
(3)将量取的浓H2SO4沿烧杯内壁慢慢注入盛有约100mL水的里,并不断搅拌,目的是。
(4)将的上述溶液沿注入中,并用50mL蒸馏水洗涤烧杯2~3次,洗涤液要中,并摇匀。
(5)加水至距刻度处,改用加水,使溶液的凹液面正好跟刻度相平。
.根据电离理论:在水溶液中电离出的___________全部是__________的化合物,叫做酸。因此酸具有通性,请用离子方程式表示下列酸的通性:
(1)盐酸溶解铁锈(Fe2O3):_________________________________________________
(2)盐酸与小苏打(NaHCO3):______________________________________________
(3)硫酸溶解氢氧化铜:____________________________________________________
(4)实验室用H2SO4和锌反应制取H2:________________________________________
.现有以下物质:
①NaCl晶体②干冰③液态的醋酸④铜⑤BaSO4固体⑥蔗糖⑦酒精
⑧熔融的KNO3 ⑨浓HNO3
回答下列问题(填序号);以上物质能导电的是____________ __________;以上物质属于非电解质的是_______________________;以上物质属于电解质的是_________________;