某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是( )

| A.Ksp[Fe(OH)3]<Ksp[Cu(OH)2] |
| B.加适量NH4Cl固体可使溶液由a点变到b点 |
| C.c、d两点代表的溶液中c(H+)与c(OH-)乘积相等 |
| D.Fe(OH)3、Cu(OH)2分别在b、c两点代表的溶液中达到饱和 |
10ml浓度为1mol/L的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减慢反应速率但又不影响氢气生成的是
| A.K2SO4 | B.CH3COONa | C.CuSO4 | D.Na2CO3 |
下列由实验现象得出的结论正确的是
| 操作及现象 |
结论 |
|
| A |
向AgCl悬浊液中加入NaI溶液时出现黄色沉淀。 |
Ksp(AgCl)< Ksp(AgI) |
| B |
向某溶液中滴加氯水后再加入KSCN溶液,溶液呈红色。 |
溶液中一定含有Fe2+ |
| C |
向NaBr溶液中滴入少量氯水和苯,振荡、静置,溶液上层呈橙红色。 |
Br—还原性强于Cl— |
| D |
加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结。 |
NH4Cl固体可以升华 |
已知常温下在溶液中可发生如下两个离子反应:Ce4+ + Fe2+ = Ce3+ + Fe3+、Sn2+ + 2Fe3+ = Sn4+ + 2 Fe2+由此可确定Ce3+、Fe2+、Sn2+三种离子的还原性强弱的顺序
| A.Sn2+、Fe2+、Ce3+ |
| B.Ce3+、Fe2+、Sn2+ |
| C.Sn2+、Ce3+、Fe2+ |
| D.Fe2+、Sn2+、Ce3+ |
下列实验操作正确的是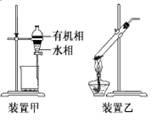
| A.用玻璃棒蘸取CH3COOH溶液点在水湿润的pH试纸上,测定该溶液的pH |
| B.中和滴定时,滴定管用所盛装的反应液润洗2~3次 |
| C.用装置甲分液,放出水相后再从分液漏斗下口放出有机相 |
| D.用装置乙加热分解NaHCO3固体 |
水溶液中能大量共存的一组离子是
| A.NH4+、Ba2+、Br-、CO32- |
| B.Cl-、SO32-、Fe2+、H+ |
| C.K+、Na+、SO42-、MnO4- |
| D.Na+、H+、NO3-、HCO3- |