某探究学习小组的同学学习氨的性质以后,为了探究氨气的某些性质,设计并进行了以下实验:
(Ⅰ)NH3的制取及收集
1.写出实验制取氨气的化学方程式 ;
2.收集氨气
(II)HCl的制取及收集
实验室通常以反应:2NaCl(晶体)+H2SO4(浓) Na2SO4 + 2HCl↑ 为原理来制取少量HCl气体,试据此分析并回答下列问题:
Na2SO4 + 2HCl↑ 为原理来制取少量HCl气体,试据此分析并回答下列问题:
1.实验室制取HCl气体可选择下列装置中的( )
A.实验室制氧气的装置 B.实验室制氢气的装置
C.实验室制二氧化碳的装置 D.实验室制氯气的装置
2.实验室制取HCl气体的反应原理遵循了以下化学反应规律中的( )
A.氧化还原反应原理
B.强酸制弱酸原理
C.难挥发性酸制取易挥发性酸
D.复分解反应原理
(III)验证氨气部分性质的探究实验:
为了同时进行氨气溶于水以及氨气与HCl的反应的探究,同学们设计了如下的实验装置图。首先在甲、乙两个干燥的圆底烧瓶中分别收集满了NH3和HCl气体,然后再按如下图所示连接好各个装置(活塞a和b均处于关闭状态),并按以下步骤进行实验:

1.先挤压胶头滴管再打开活塞b,请你预测此时乙中可能观察到的现象是: ______ 。
发生反应的方程式为: 。
2.待乙中观察到明显现象后立即关闭活塞b,并打开活塞a,又将可能观察到的实验现象是: 。
下列实验操作不正确的是 _。
| A.在催化剂存在的条件下,苯和溴水发生反应可生成无色、比水重的液体溴苯 |
| B.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,完成乙醇氧化为乙醛的实验 |
| C.醇中含有少量水可加入硫酸铜再蒸馏制得无水乙醇 |
| D.试管中先加入一定量浓硫酸,再依次加入适量冰醋酸、乙醇,然后加热制取乙酸乙酯 |
E.实验室制取乙烯时,放入几片碎瓷片,以避免混合液在受热沸腾时剧烈跳动
F.配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
G.验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置、待液体分层后,滴加硝酸银溶液
(12分)(1)写出实验室由苯和浓硝酸反应制取硝基苯的化学
方程式:该反应属于反应。
(2)右图所示的实验装置图中存在哪些错误?请指正。
①;
②;
③。
(3)在试管中将两种浓酸混和的操作方法是。
(15分)“套管实验”是将一支较小的试管装入另一试管中,经组装来完成原来需要两只或更多试管进行的实验。因其有许多优点,近年来被广泛开发并应用于化学实验中。下面这个实验为“套管实验”,实验装置如下图,小试管中部有沾上无水硫酸铜粉末的脱脂棉。请观察实验装置,分析实验原理,并回答下列问题:
(1)整个实验过程中,能观察到的现象为
①烧杯A中________;②小试管中________;
③烧杯B中____________________________;
(2)实验结束时,在操作上要特别注意的问题是
____________________________________________________________________
(3)写出实验过程中发生反应的化学方程式
某同学设计如图所示装置分别进行探究实验(夹持装置已略去),请回答下列问题: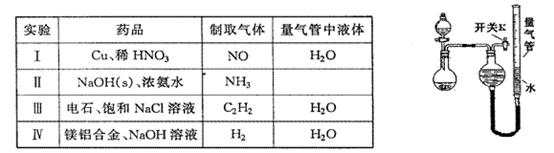
(1)如何检验如图所示装置的气密性:。
(2)该同学认为实验I可通过收集并测量NO气体的体积来探究铜样品的纯度,你认为是否可行?(填“可行”或“不可行”),原因是。
(3)实验Ⅲ烧瓶中发生反应的化学方程式是,打开开关K,产生的气体经验纯后点燃,现象是。
(4)实验Ⅱ中量气管中的液体最好是____(填字母编号,下同)
a.浓NaOH溶液 b.氨水 c.煤油 d.饱和氯化铵溶液
该实验剩余的NH3需吸收处理。以下各种尾气吸收装置中,适合于吸收NH3,而且能防止倒吸的有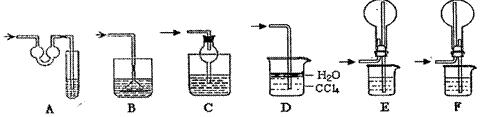
(5)本实验应对量气管多次读数,读数时应注意:①将实验装置恢复到室温,②,③视线与凹液面最低处相平。
(6)实验Ⅳ获得以下数据(所有气体体积均已换算成标准状况,忽略滴入液体体积对气体体积的影响)
| 编号 |
镁铝合金质量 |
量气管第一次读数 |
量气管第二次读数 |
| ① |
1.0g |
10.0mL |
346.3mL |
| ② |
1.0g |
10.0mL |
335.0mL |
| ③ |
1.0g |
10.0mL |
345.7mL |
根据上述数据,可计算出镁铝合金中铝的质量分数为__。
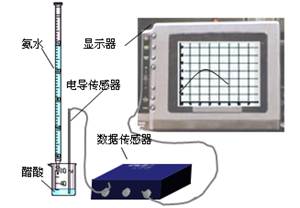
DIS系统即数字化信息 系统,它由传感器、数据采集器和计算机组成,某研究性学习小组用DIS系统测定食用白醋中醋酸的物质的量浓度,以溶液的导电能力来判断滴定终点。实验步骤如下:
系统,它由传感器、数据采集器和计算机组成,某研究性学习小组用DIS系统测定食用白醋中醋酸的物质的量浓度,以溶液的导电能力来判断滴定终点。实验步骤如下:
⑴用_______________(填仪器名称)量取10.00mL食用白醋,在_________(填仪器名称)中用水稀释后转移到100mL___________(填仪器名称)中定容,然后将稀释后的溶液倒入试剂瓶中。
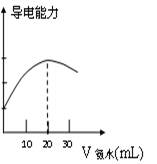
⑵量取20.00mL上述溶液倒入烧杯中,连接好DIS系统(见左下图),向烧杯中滴加浓度为0.1000mol/L的氨水,计算机屏幕上显示出溶液导电能力随氨水体积变化的曲线(见右下图)。
①用滴定管盛氨水前,滴定管要用_________润洗2~3遍,润洗的目的是____________。
②氨水与醋酸反应的离子方程式是_ ________________________
________________________ _________________。
_________________。
③食用白醋中醋酸的物质的量浓度是_____________。